2020年07月09日,国家药品监督管理局组织制定了《一次性使用乳腺定位丝注册技术审查指导原则》《硬脑(脊)膜补片注册技术审查指导原则》《定制式个性化骨植入物等效性模型注册技术审查指导原则》《骨科金属植入物有限元分析资料注册技术审查指导原则》《疝修补补片临床试验指导原则》《生物可吸收冠状动脉药物洗脱支架动物实验研究指导原则》,旨在加强医疗器械产品注册工作的监督和指导,进一步提高注册审查质量。为更好的帮助您梳理内容,小编已选择两个具有代表性的指导原则为您深度解读,《硬脑(脊)膜补片注册技术审查指导原则》(以下简称《补片》)和《生物可吸收冠状动脉药物洗脱支架动物实验研究指导原则》(以下简称《支架》),快随小编一睹为快吧!
《补片》:硬脑(脊)膜补片是指用于硬脑膜和/或硬脊膜缺损修补的片状材料类产品。材质涵盖聚四氟乙烯/聚氨酯类等不可吸收合成材料、聚乳酸/聚己内酯等可吸收合成材料、动物源性材料、同种异体材料及不同材料的组合等。
《支架》:适用于平台为高分子材料的生物可吸收支架的动物实验研究。对于其他产品,如支架中含有生物技术成分以及其他生物可吸收材料支架平台如镁合金或铁合金等制成的支架,可参考本指导原则中适用的内容开展动物实验。
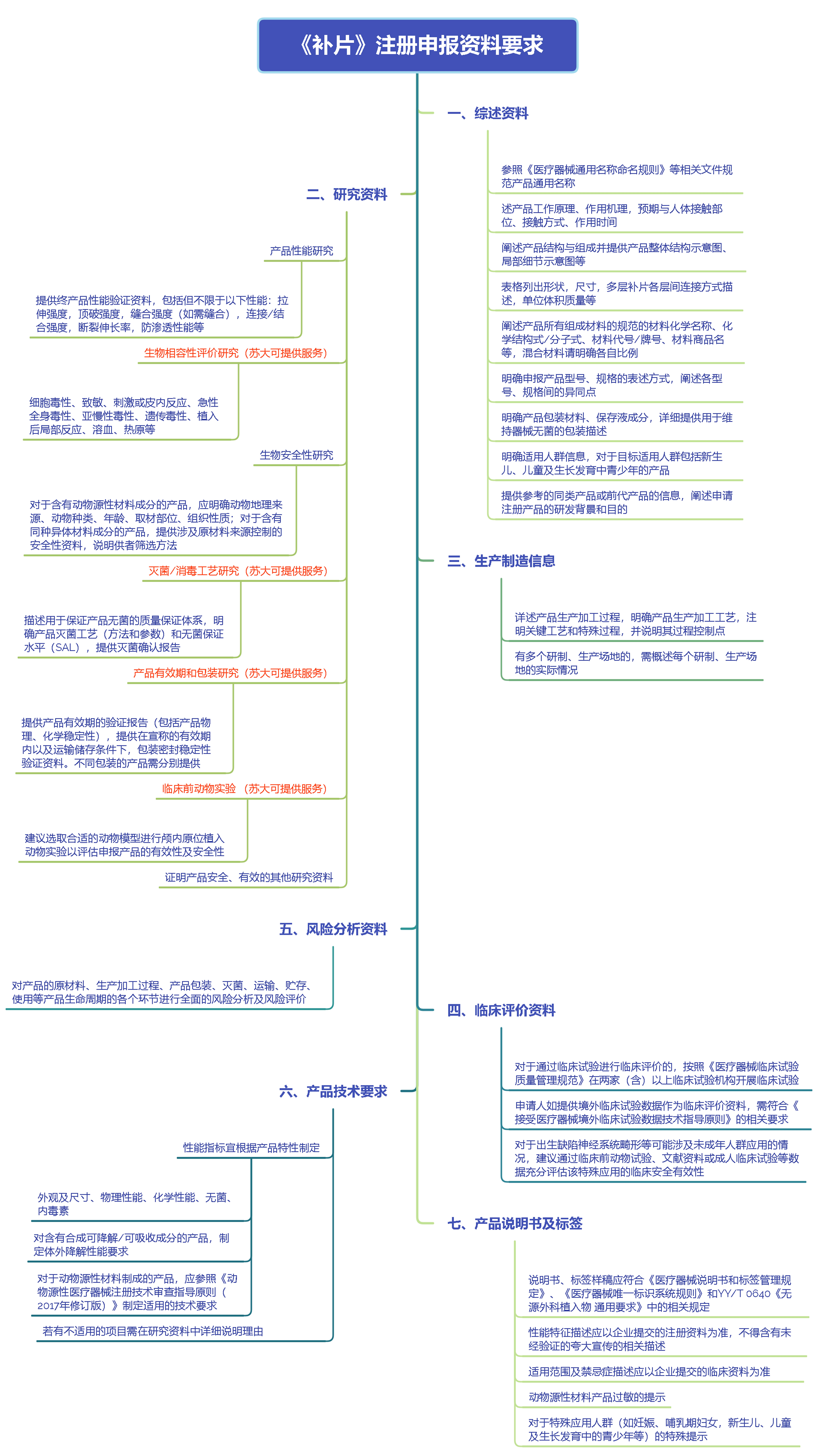
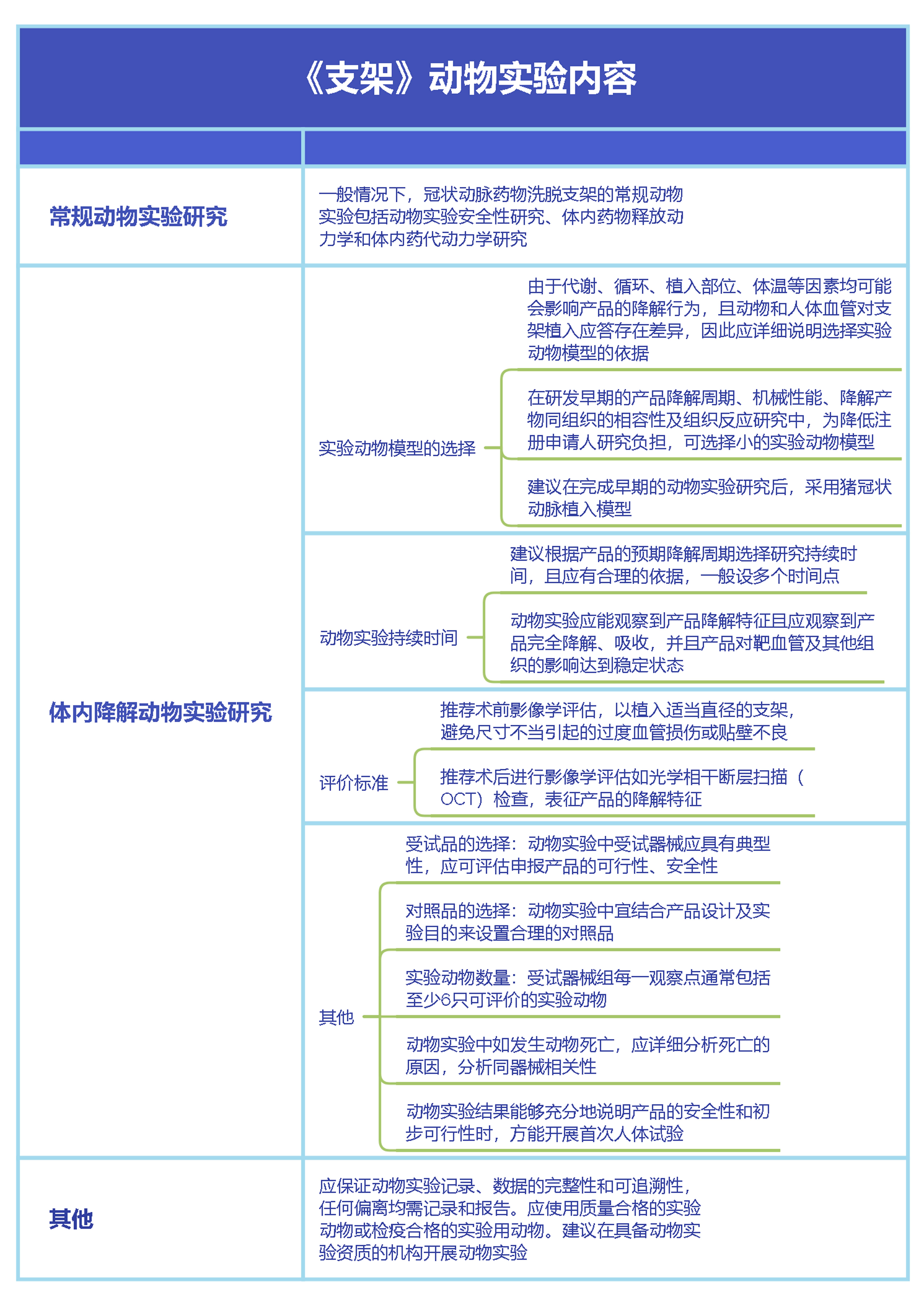
二、《补片》注册申报资料要求和《支架》动物实验内容
原文链接:http://www.nmpa.gov.cn/WS04/CL2138/378635.html
【原文来源】国家药品监督管理局
【全文整理】苏州大学卫生与环境技术研究所
【声明】如果您认为我们的内容或来源标注与原文不符,请告知我们,我们将与您积极协商解决。谢谢大家的关注!