摘要:8月NMPA、CMDE发布的法规通告汇总
合集:#法规汇总
公告
为进一步规范电子内窥镜医疗器械的管理,国家药监局器审中心组织制定了《电子内窥镜同品种临床评价注册审查指导原则》,现予发布。
特此通告。
原文链接:国家药监局器审中心关于发布电子内窥镜同品种临床评价注册审查指导原则的通告(2023年第35号) (cmde.org.cn)
为做好医疗器械注册受理前技术问题咨询工作,指导行政相对人安排咨询时间,保证咨询工作质量,现就近期咨询工作安排通告如下:
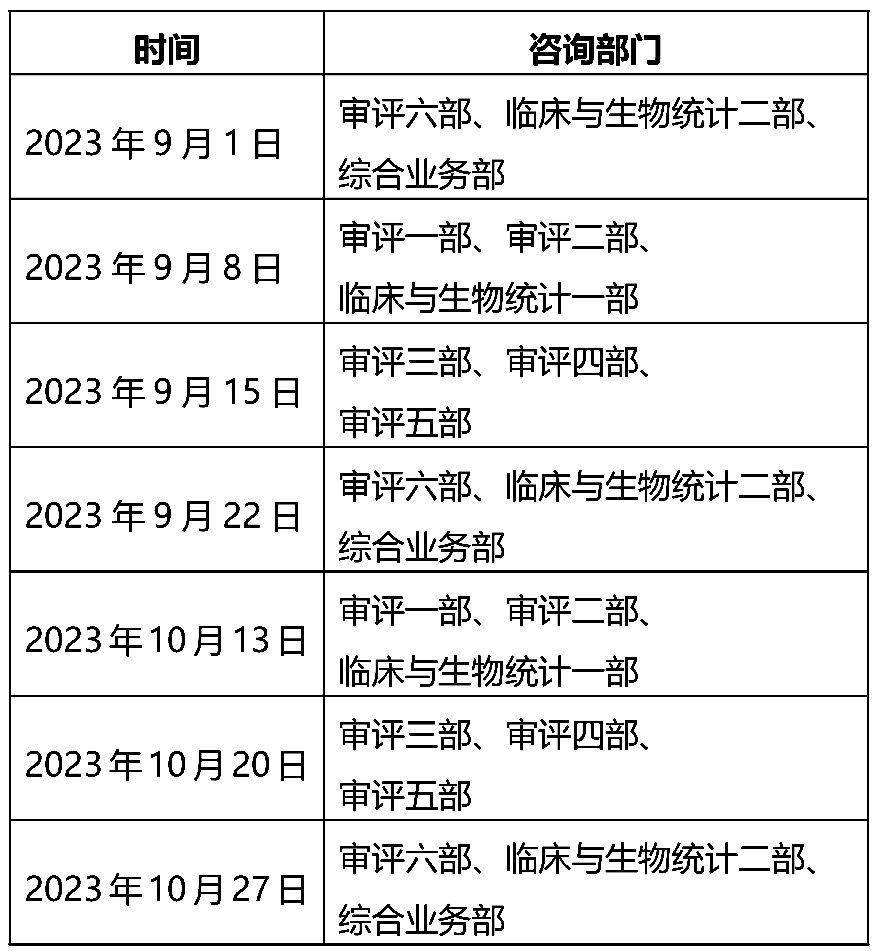
注:受理前咨询工作暂时采用视频会议方式进行,申请人预约成功后请等待电话通知。请申请人按照我中心2022年10月16日发布的《关于医疗器械受理前技术问题咨询工作安排调整的通告》(2022年第37号)的要求申请和办理,各受理前技术问题咨询参与单位咨询时间安排同器审中心,但不受轮值部门限制。
原文链接:关于2023年9月~10月医疗器械注册受理前技术问题咨询工作安排的通告(2023年第34号) (cmde.org.cn)
依据国家药品监督管理局《创新医疗器械特别审查程序》(国家药监局2018年第83号公告)要求,创新医疗器械审查办公室组织有关专家对创新医疗器械特别审查申请进行了审查,拟同意以下申请项目进入特别审查程序,现予以公示。
1.产品名称:心脏冷冻消融系统
申请人:上海安钛克医疗科技有限公司
2.产品名称:植入式心脏复律除颤器
申请人:苏州无双医疗设备有限公司
3.产品名称:一次性使用压力监测脉冲电场消融导管
申请人:四川锦江电子医疗器械科技股份有限公司
4.产品名称:一次性使用磁电定位压力监测脉冲电场消融导管
申请人:湖南埃普特医疗器械有限公司
5.产品名称:脉冲电场消融设备
申请人:深圳迈微医疗科技有限公司
6.产品名称:近红外光脑功能治疗仪
申请人:丹阳慧创医疗设备有限公司
7.产品名称:颅内动脉瘤介入手术仿真软件
申请人:西姆医疗公司
8.产品名称:人CDO1/AJAP1/GALR1基因甲基化检测试剂盒(荧光PCR法)
申请人:武汉凯德维斯生物技术有限公司
9.产品名称:光固化创面封闭胶
申请人:中山光禾医疗科技有限公司
公示时间:2023年8月23日至2023年9月6日
公示期内,任何单位和个人有异议的,可以书面、电话、邮件等方式向我中心综合业务部反映。
联系人:张欣
电话:010-86452928
电子邮箱:gcdivision@cmde.org.cn
地址:北京市海淀区气象路50号院1号楼
特别说明:进入创新审查程序不代表已认定产品具备可获准注册的安全有效性,申请人仍需按照有关要求开展研发及提出注册申请,药品监督管理部门及相关技术机构将按照早期介入、专人负责、科学审查的原则,在标准不降低、程序不减少的前提下进行审评审批。
原文链接:创新医疗器械特别审查申请审查结果公示(2023年第6号) (cmde.org.cn)
为进一步规范软性接触镜医疗器械的管理,国家药监局器审中心组织制定了《软性接触镜临床评价注册审查指导原则》,现予发布。
特此通告。
原文链接:国家药监局器审中心关于发布软性接触镜临床评价注册审查指导原则的通告(2023年第33号) (cmde.org.cn)
为进一步规范牙科种植体系统医疗器械的管理,国家药监局器审中心组织制定了《牙科种植体系统同品种临床评价注册审查指导原则》,现予发布。
特此通告。
原文链接:国家药监局器审中心关于发布牙科种植体系统同品种临床评价注册审查指导原则的通告(2023年第32号) (cmde.org.cn)
为进一步规范正电子发射/X射线计算机断层成像系统的管理,国家药监局器审中心组织制定了《正电子发射/X射线计算机断层成像系统同品种临床评价注册审查指导原则》,现予发布。
特此通告。
原文链接:国家药监局器审中心关于发布正电子发射/X射线计算机断层成像系统同品种临床评价注册审查指导原则的通告(2023年第31号) (cmde.org.cn)
为进一步规范医用X射线诊断设备(第三类)的管理,国家药监局器审中心组织制定了《医用X射线诊断设备(第三类)同品种临床评价注册审查指导原则》,现予发布。
特此通告。
原文链接:国家药监局器审中心关于发布医用X射线诊断设备(第三类)同品种临床评价注册审查指导原则的通告(2023年第30号) (cmde.org.cn)
为进一步规范血液透析浓缩物医疗器械的管理,国家药监局器审中心组织制定了《血液透析浓缩物临床评价注册审查指导原则》,现予发布。
特此通告。
原文链接:国家药监局器审中心关于发布血液透析浓缩物临床评价注册审查指导原则的通告(2023年第29号) (cmde.org.cn)
YY 0068.4-2009《医用内窥镜硬性内窥镜 第4部分:基本要求》等7项医疗器械行业标准修改单已经审定通过,现予以公布。标准修改单内容及实施日期见附件。
特此公告。
原文链接:国家药监局关于发布YY 0068.4-2009《医用内窥镜硬性内窥镜 第4部分:基本要求》等7项行业标准修改单的公告(2023年第107号) (nmpa.gov.cn)
2023年7月,国家药监局共批准注册医疗器械产品197个。其中,境内第三类医疗器械产品150个,进口第三类医疗器械产品21个,进口第二类医疗器械产品21个,港澳台医疗器械产品5个(具体产品见附件)。
特此公告。
原文链接:国家药监局关于批准注册197个医疗器械产品的公告(2023年7月)(2023年第106号) (nmpa.gov.cn)
为完善药品监管信息化标准体系,促进医疗器械监管信息共享和数据协同,我局依据《医疗器械监督管理条例》《医疗器械注册与备案管理办法》《体外诊断试剂注册与备案管理办法》等规定,组织制订了《医疗器械注册与备案管理基本数据集》《体外诊断试剂注册与备案管理基本数据集》《医疗器械(含体外诊断试剂)监管信息基础数据元(注册和备案部分)》《医疗器械(含体外诊断试剂)监管信息基础数据元值域代码(注册和备案部分)》等4个信息化标准(见附件)。现予发布,自发布之日起实施。
特此公告。
原文链接:国家药监局关于发布《医疗器械注册与备案管理基本数据集》等4个信息化标准的公告(2023年第103号) (nmpa.gov.cn)
为贯彻落实《药品管理法》《疫苗管理法》《医疗器械监督管理条例》《化妆品监督管理条例》,加强药品、医疗器械和化妆品监管信息化标准的统筹规划和体系建设,提升药品监管数字化水平和监管数据共享效能,根据《药品监管网络安全与信息化建设“十四五”规划》要求,国家药监局组织制定了《药品监管信息化标准体系》,现予发布,自发布之日起实施。原国家食品药品监督管理总局CFDAB/T 0101-2014《食品药品监管信息化标准体系》同时废止。
特此公告。
原文链接:国家药监局关于发布《药品监管信息化标准体系》的公告(2023年第97号) (nmpa.gov.cn)
为进一步深化医疗器械审评审批制度改革,依据医疗器械产业发展和监管工作实际,按照《医疗器械监督管理条例》《医疗器械分类目录动态调整工作程序》有关要求,国家药监局决定对《医疗器械分类目录》部分内容进行调整。
原文链接:国家药监局关于调整《医疗器械分类目录》部分内容的公告(2023年第101号) (nmpa.gov.cn)
征集
1. 【CMDE】关于公开征求《一次性使用膜式氧合器(CPB用)注册审查指导原则(征求意见稿)》和《透析液过滤器注册审查指导原则(征求意见稿)》意见的通知
– 2023.8.2
各有关单位:
我中心结合医疗器械注册法规、境内外注册申报产品的特点及申报现状,在总结技术审评实际情况,并参考相关文献资料的基础上,对已经发布实施的一次性使用膜式氧合器审查指导原则进行了修订,形成《一次性使用膜式氧合器(CPB用)注册审查指导原则(征求意见稿)》。同时新制定了《透析液过滤器注册审查指导原则(征求意见稿)》,现向社会公开征求意见。请将反馈意见以电子邮件的形式于2023年9月9日前反馈我中心。
联系人:骆庆峰 杨宇希 蔡娜娜
电话:010-86452840、86452833、86452873
电子邮箱:luoqf@cmde.org.cn
通讯地址:北京市海淀区气象路50号院1号楼国家药品监督管理局医疗器械技术审评中心
邮编:100081
原文链接: 关于公开征求《一次性使用膜式氧合器(CPB用)注册审查指导原则(征求意见稿)》和《透析液过滤器注册审查指导原则(征求意见稿)》意见的通知 (cmde.org.cn)



