欧盟健康和数字执行机构(HaDEA)研究显示大多数MDR下的申请处理时间(从申请到书面协议的签署)为1~3个月。基于此,Team-NB于2024年12月18日发布MDR认证流程(包括预申请、申请和申请后阶段)的共识文件,为进行MDR认证的制造商提供详细的申请流程,有助于减少不完整的申请,提高公告机构(NB)处理申请的效率,加速制造商MDR认证。
目的和范围
本文件旨在详细描述预申请和申请流程,制造商可通过这些流程向NB 申请MDR 法规下的医疗器械认证。本文件既适用于根据MDR Art.120过渡到 MDR 的遗留器械,也适用于新进入市场且尚未根据指令获得认证的器械。本文件还简要介绍了申请程序结束后开展的认证活动。
以下内容不属于本文件的范围:
- 根据MDR Art. 16申请NB证书的程序;
- 根据MDR Art.117申请 NB 意见的程序;
- 根据MDR Annex VII §4.11 申请再认证的程序。
认证流程各阶段
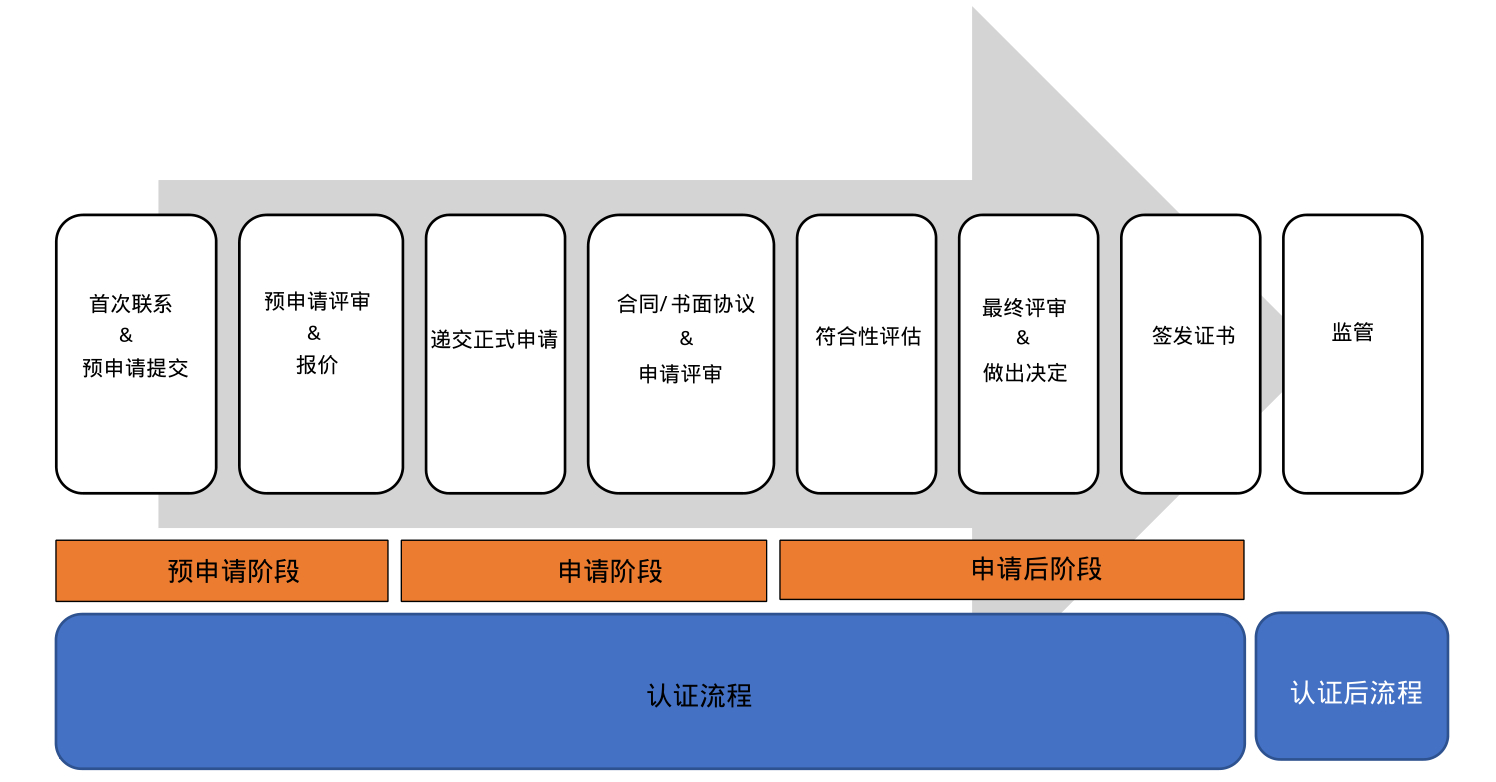
MDR认证流程主要分为预申请阶段、申请阶段和申请后阶段,共8个环节。
首次联系和预申请提交
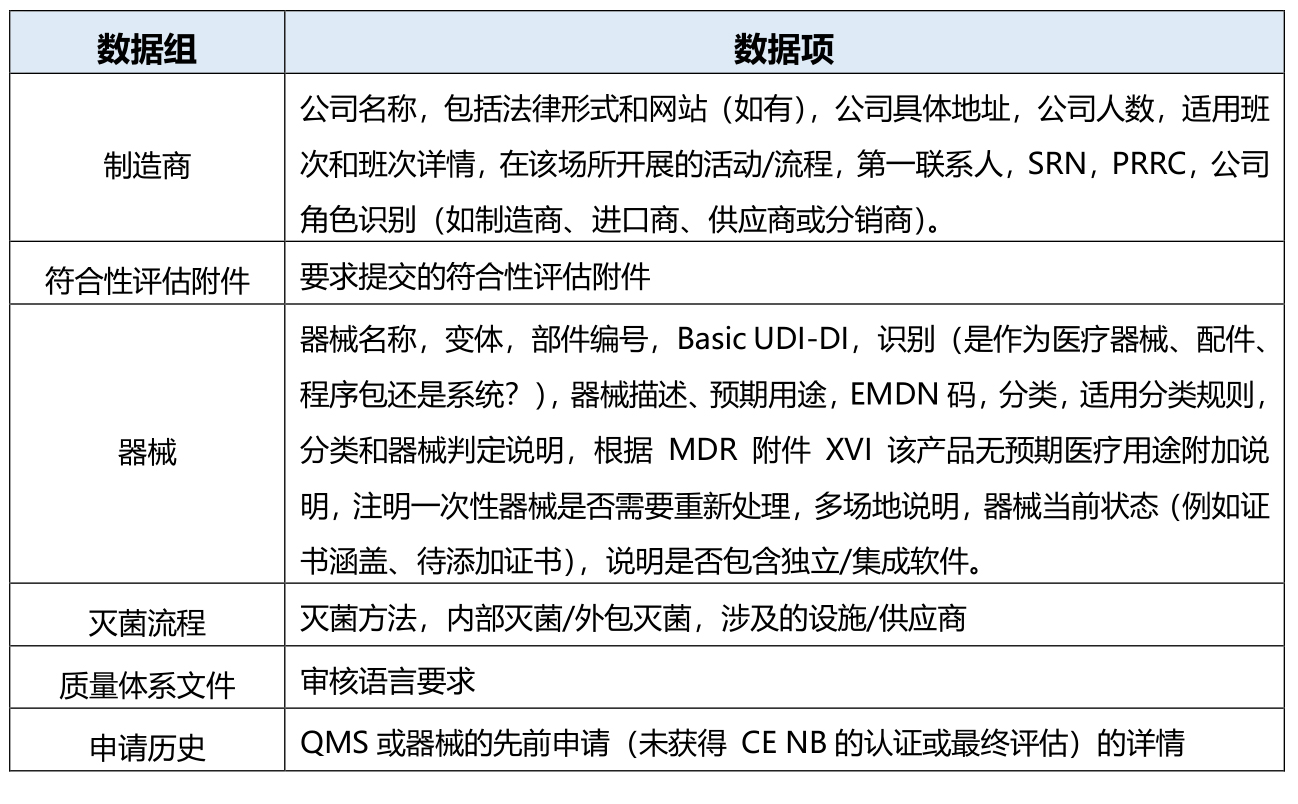
制造商首次向NB提出关于医疗器械的符合性评估服务既可以通过口头的,也可通过电子邮件或在线表单等数字化形式。MDR要求NB在向制造商发出任何报价之前,对预申请信息进行审查,包括初步核实产品是否属于MDR的范围及分类。根据这一要求,制造商应在预申请阶段向NB提供以下信息:
预申请评审和报价
NB根据制造商提供的上表信息进行审核,确认产品是否符合MDR的范围及其分类是否正确。基于审核结果,NB将向制造商提供报价单,并可能会要求提供补充信息或说明,来确保报价的准确性。若预申请信息或获得的补充信息导致最初报价的变化,NB则可在申请评审或符合性评估的后续阶段征得制造商同意后对报价进行修改。
递交正式申请
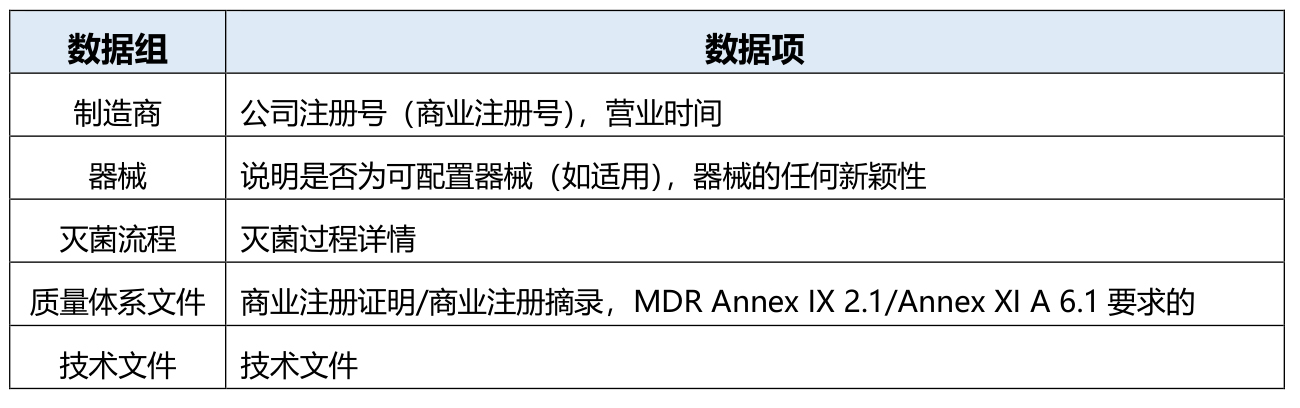
若制造商对报价无异议并打算继续申请程序,则至少应向NB提交QMS相关文件及技术文件的全文/章节/摘要(视器械类别而定),具体信息见下表:
合同/书面协议和申请评审
一旦提交申请,NB将向制造商提供合同文件,双方签署后即达成书面协议,开始申请评审。评审的内容包括申请的完整性、产品资格、分类、符合性评估程序是否适用于申请器械等。根据申请评审结果,NB将决定接受申请还是拒绝申请(仅在签订合同后)。任何拒绝申请的决定都会在EUDAMED或通过其他方式(如果不使用EUDAMED)通知。同样,如果制造商在此阶段决定撤回申请,则NB也将会在相关网站上通知撤回情况。如果制造商希望在申请中增加一种新产品,而该产品不属于原始申请和相关书面协议的一部分,则NB可要求就新产品提交一份新申请。如果制造商希望对已经提交给NB的申请进行修改,则应与NB联系讨论是否允许进行这些修改、提交这些修改的程序以及对现有申请的任何影响。



