公告
1.【NMPA】关于发布YY/T 0910.2—2025《医用电气设备医学影像显示系统 第2部分:医学影像显示系统的验收和稳定性试验》等15项推荐性医疗器械行业标准的公告(2025年第106号)- 2025.10.30
YY/T 0910.2—2025《医用电气设备医学影像显示系统 第2部分:医学影像显示系统的验收和稳定性试验》等15项推荐性医疗器械行业标准已经审定通过,现予以公布。标准编号、标准名称、适用范围和实施日期见附件。
特此公告。
原文链接:国家药监局关于发布YY/T 0910.2—2025《医用电气设备医学影像显示系统 第2部分:医学影像显示系统的验收和稳定性试验》等15项推荐性医疗器械行业标准的公告(2025年第106号)
2.【NMPA】关于发布国家医疗器械监督抽检结果的通告(2025年第38号)- 2025.10.29
为加强医疗器械监督管理,保障医疗器械产品质量安全有效,国家药品监督管理局组织对半导体激光治疗机、聚氨酯泡沫敷料等10个品种进行了产品质量监督抽检,有14批(台)产品不符合标准规定。具体情况通告请点击原文链接。
原文链接:国家药监局关于发布国家医疗器械监督抽检结果的通告(2025年第38号)
3.【CMDE】关于创新医疗器械特别审查申请审查结果公示(2025年第10号)- 2025.10.29
依据国家药品监督管理局《创新医疗器械特别审查程序》(国家药监局2018年第83号公告),创新医疗器械审查办公室组织有关专家对创新医疗器械特别审查申请进行审查,拟同意以下申请项目进入特别审查程序,现予以公示。公示时间为2025年10月29日至11月12日,具体公示产品请点击原文链接。
原文链接:创新医疗器械特别审查申请审查结果公示(2025年第10号)
4.【NMPA】关于批准注册348个医疗器械产品的公告(2025年9月)(2025年第103号)- 2025.10.17
2025年9月,国家药监局共批准注册医疗器械产品348个。其中,境内第三类医疗器械产品276个,进口第三类医疗器械产品34个,进口第二类医疗器械产品36个,港澳台医疗器械产品2个(具体产品信息请点击原文链接)。
特此公告。
原文链接:国家药监局关于批准注册348个医疗器械产品的公告(2025年9月)(2025年第103号)
5.【CMDE】关于2025年11月~12月医疗器械注册受理前技术问题咨询工作安排的通告(2025年第24号)- 20210.15
为做好医疗器械注册受理前技术问题咨询工作,指导行政相对人安排咨询时间,保证咨询工作质量,现就近期咨询工作安排通告如下:
一、轮值部门时间安排:
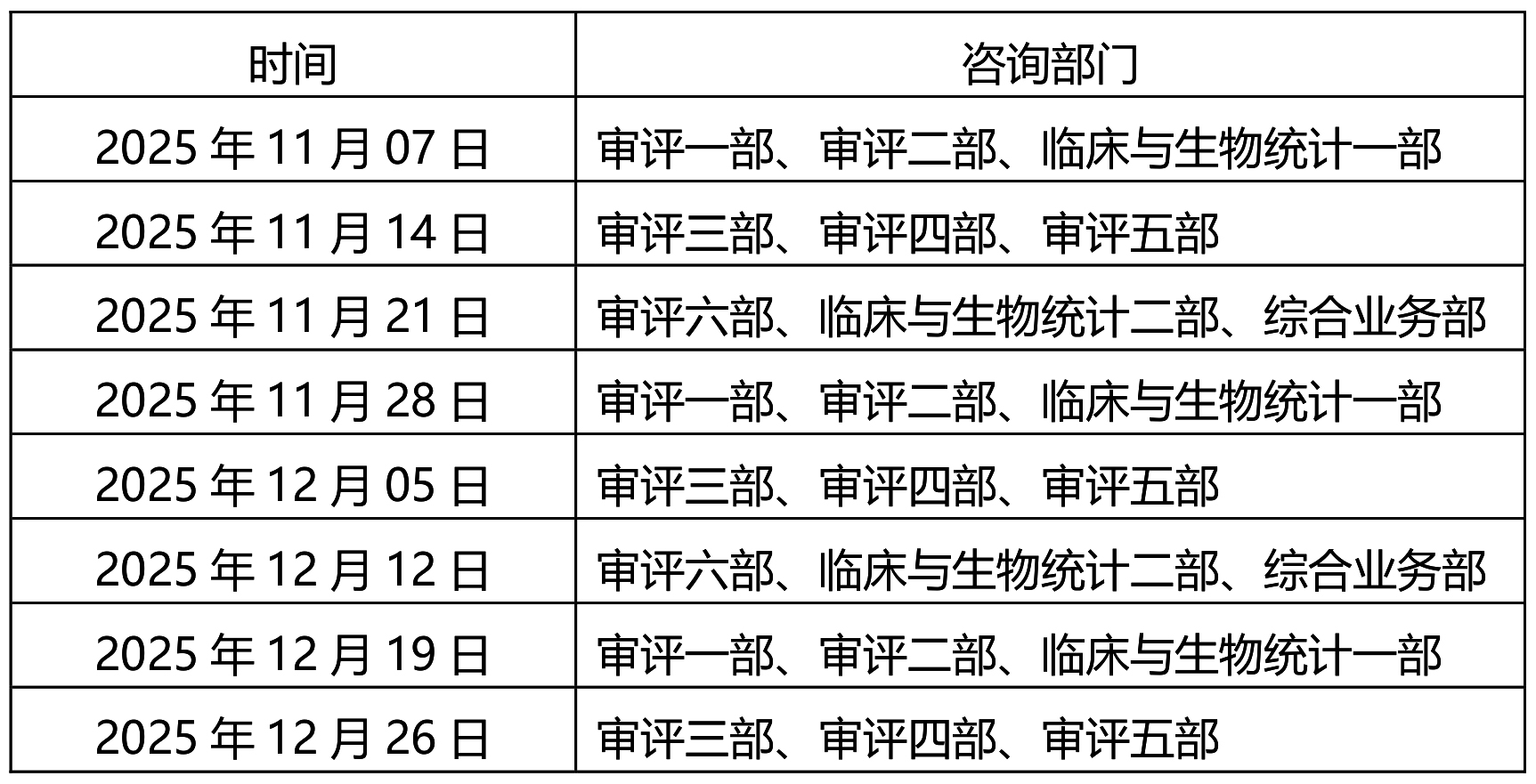 二、自2024年11月起,每个受理前技术问题咨询日各审评部、临床部、综合业务部可供预约的现场咨询号数量为20个,预约方式不变。按照中心2022年10月16日发布的《关于医疗器械受理前技术问题咨询工作安排调整的通告》(2022年第37号)的要求申请和办理。未预约现场咨询或预约未成功的单位,可选择邮件方式提交咨询申请。各受理前技术问题咨询参与单位咨询时间安排同器审中心,但不受轮值部门限制。
二、自2024年11月起,每个受理前技术问题咨询日各审评部、临床部、综合业务部可供预约的现场咨询号数量为20个,预约方式不变。按照中心2022年10月16日发布的《关于医疗器械受理前技术问题咨询工作安排调整的通告》(2022年第37号)的要求申请和办理。未预约现场咨询或预约未成功的单位,可选择邮件方式提交咨询申请。各受理前技术问题咨询参与单位咨询时间安排同器审中心,但不受轮值部门限制。
咨询时间:工作日每周五下午1:30至4:30(法定节假日除外),请申请人于下午3:00前取号。
咨询地点:北京经济技术开发区广德大街22号院一区2号楼一层。
原文链接:关于2025年11月~12月医疗器械注册受理前技术问题咨询工作安排的通告(2025年第24号)
6.【CMDE】关于发布一次性使用麻醉用针注册审查指导原则的通告(2025年第23号)- 2025.10.11
为进一步规范一次性使用麻醉用针的管理,国家药监局器审中心组织制定了《一次性使用麻醉用针注册审查指导原则》,现予发布。
特此通告。
原文链接:国家药监局器审中心关于发布一次性使用麻醉用针注册审查指导原则的通告(2025年第23号)
征集
各有关单位:
根据国家药品监督管理局医疗器械注册审查指导原则制修订计划的有关要求,我中心组织修订了《腔镜用吻合器产品注册技术审查指导原则》(2017年第44号),形成了《腔镜吻合器注册审查指导原则(2025年修订版)(征求意见稿)》(附件1),现向社会公开征求意见。
如有意见或建议,请填写反馈意见表(附件2),并于2025年11月17日前将意见反馈至联系人邮箱。
原文链接:关于公开征求《腔镜吻合器注册审查指导原则(2025年修订版)(征求意见稿)》意见的通知
各有关单位:
为进一步加强医疗器械注册审查指导原则在注册申报和技术审评工作中的指导作用,根据国家药品监督管理局医疗器械技术审评中心2025年度注册审查指导原则编制计划的有关要求,我中心已启动《乳房旋切穿刺针及配件注册审查指导原则》制订工作。现征集参与单位,邀请具有相关工作经验的境内外生产企业、科研机构、临床机构等积极参与。
请有意向参与修订及编制工作的单位填写参与单位信息征集表(见附件),于2025年11月14日前统一以电子版形式报送我中心
原文链接:关于征集《乳房旋切穿刺针及配件注册审查指导原则》制订工作参与相关企业及单位信息的通知



