原材料是医疗器械产品实现其预期功能的重要载体,也是其安全性和有效性的重要保障,使得医疗器械原材料变化的变更控制在各项变更事项中显得尤为重要。因此,当生产产品所用的原材料发生变化时,注册人应充分评估原材料变化对最终医疗器械产品可能带来的影响,以将变化引起的风险降低至可接受范围,并根据法规要求评估是否需要进行注册审批。
5月19日,国家药监局发布了《无源医疗器械产品原材料变化评价指南》(以下简称《指南》)(2020年第33号通告),旨在给出系统的、具有指导意义的无源医疗器械产品原材料变化进行风险分析的指南性文件,用于指导注册人规范相关产品的设计开发、注册申报及质量控制,同时也用于指导监管部门对相关无源医疗器械原材料变化引起的注册申请的技术审评。
敲黑板,划重点
一、适用范围
1、仅适用于无源医疗器械产品原材料变化
2、无源医疗器械初包装材料改变可参考
3、有源医疗器械中的无源组件原材料改变可参考
4、无源医疗器械因生产工艺的改变而带来最终产品的生物相容性和/或物理化学特性等的改变可参考
二、基本原则
风险管理贯穿于医疗器械生产质量管理体系全过程,变更控制也应符合医疗器械生产质量管理体系中风险管理的要求,特别是风险分析、风险评价、风险控制以及再评价等。
三、变更决策评估路径
1.风险识别依据:医疗器械自身的特性和预期用途,医疗器械安全有效基本要求清单、设计开发及变更控制程序要求等相关文件。
2.评价手段:已有数据及信息的搜集论证、实验室研究、生物学评价等,必要时还应通过动物实验甚至临床评价进行论证。
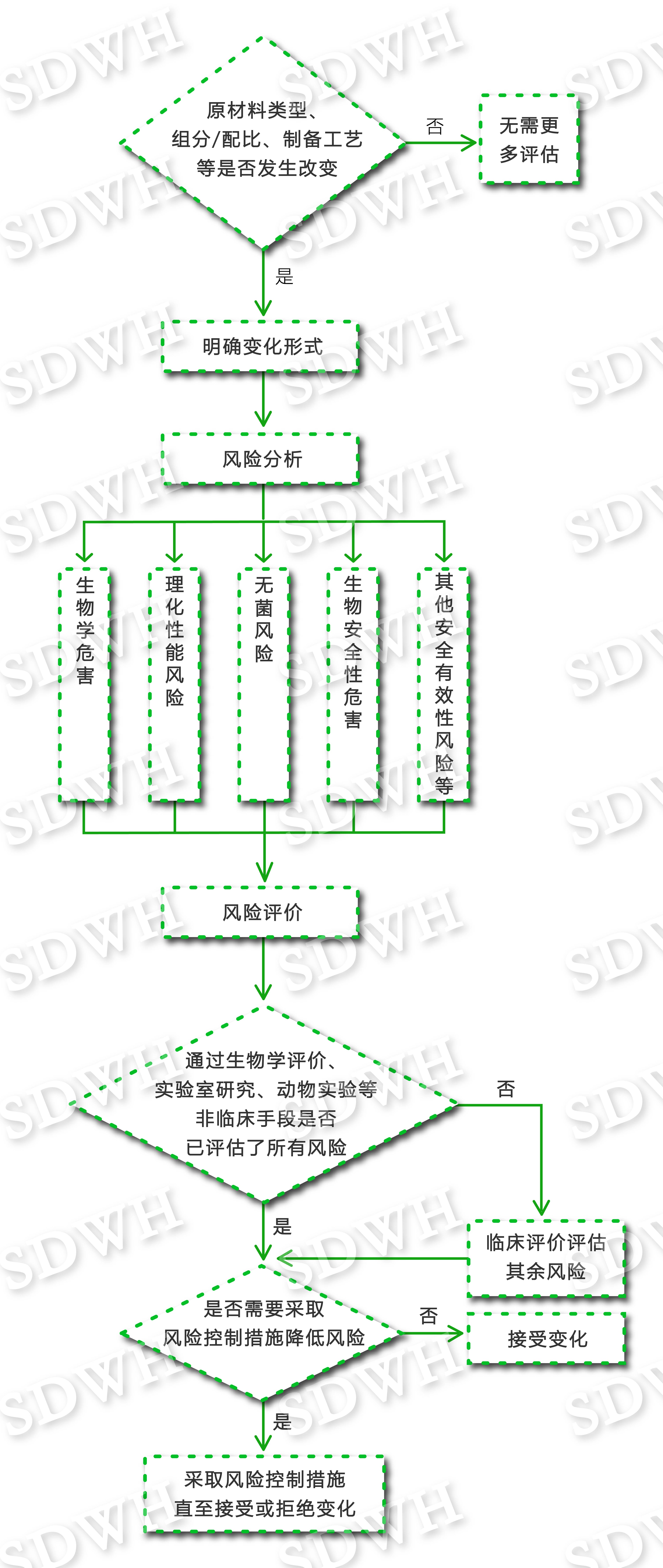
3.对医疗器械材料改变带来的风险进行评估的常用路径:
判断材料变化形式à生物学评价à实验室研究à动物实验及临床评价à风险评价及控制
4.评价终点:风险可以接受。当风险被评价为不能接受时应制定措施降低或控制风险,甚至拒绝原材料变化。
5.变更后:继续通过不良事件监测等手段对医疗器械风险信息进行收集、评价、干预、控制,最大限度地控制医疗器械潜在的风险。
附录1
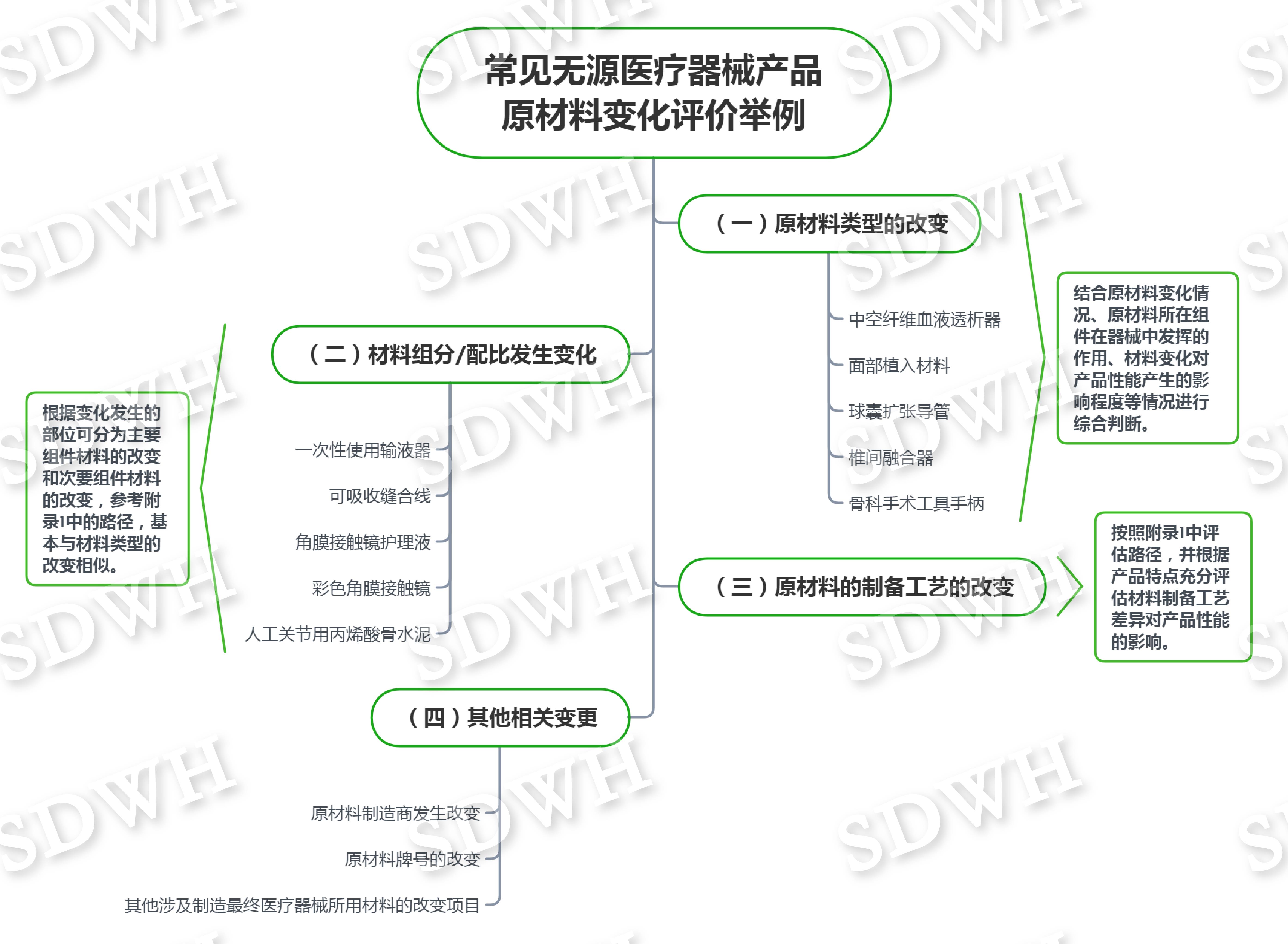
附录2
扫码查看原文

【文章来源】国家药监局
【全文整理】苏州大学卫生与环境技术研究所
【声明】如果您认为我们的内容或来源标注与原文不符,请告知我们,我们将与您积极协商解决。谢谢大家的关注。
【免责声明】
如果您认为我们的内容或来源标注与原文不符,请告知我们,我们将与您积极协商解决。谢谢大家的关注。