国际疫情持续蔓延,国内口罩等医疗物资出口热度逐步加大,为了更好的规范指导生产企业走向欧洲市场,国家市场监督管理总局于2020年05月04日出台公告,发布《口罩等防疫用品出口欧盟准入信息指南(第三版)》,涵盖“欧盟上市销售医疗器械的符合性声明”、“欧盟授权代表”、“国内具备欧盟公告机构口罩等业务资质的认证机构名录”、“国内可以开展医疗器械管理体系(ISO13485)认证的机构名录(更新至2020年4月30日)”四个大类。
一、医械产品如何加贴CE标志?
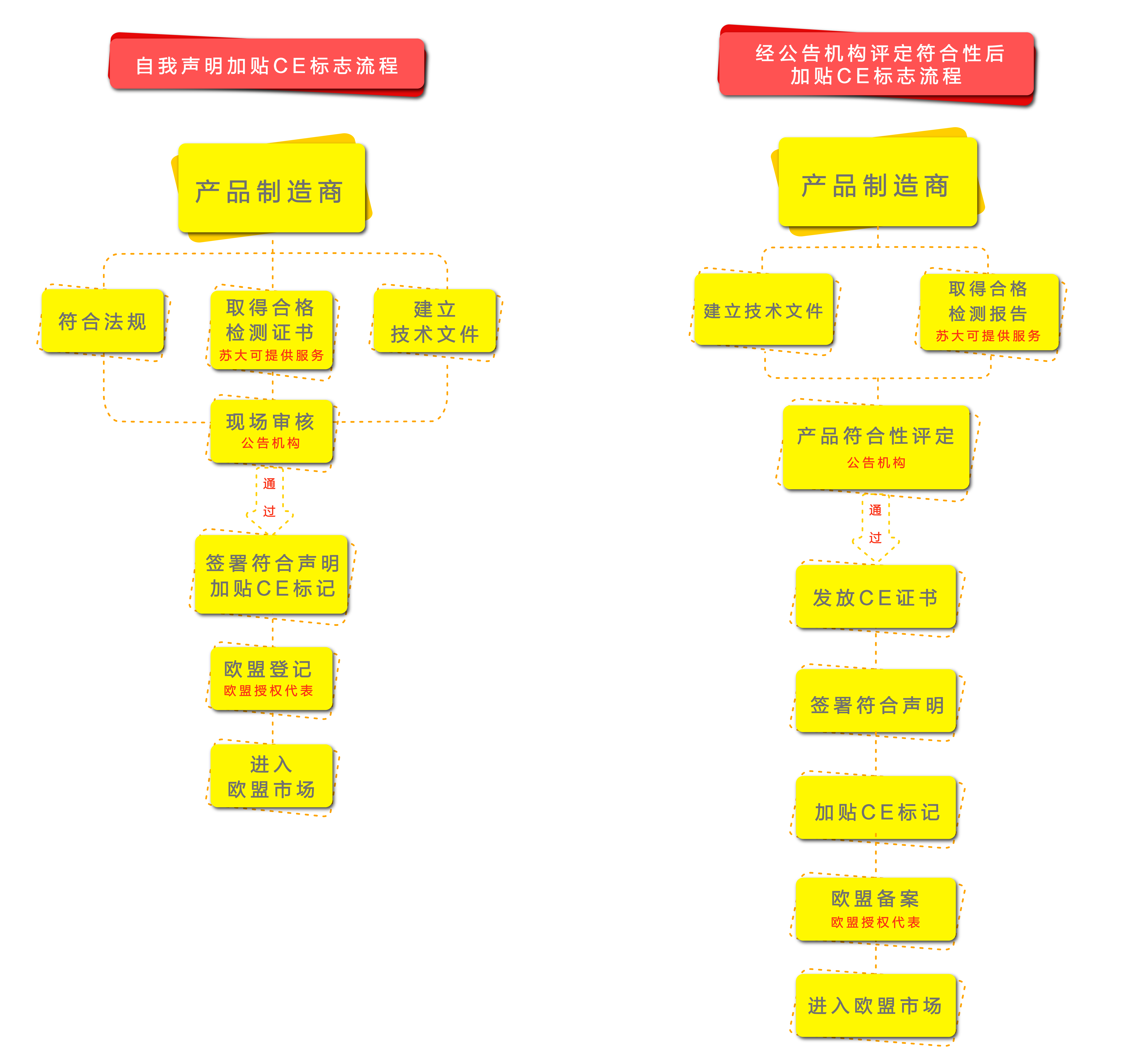
产品想要进入欧盟市场,首先要取得CE标志,这是欧盟统一的监管方式。只有符合欧盟有关安全、健康、环保等法规要求的产品,才能加贴CE标志,也意味着该产品可以在欧盟成员国、欧洲贸易自由区、以及英国和土耳其合法上市销售。根据欧盟规定,按照不同产品的不同评价方式,加贴CE标志的方式主要分为两类:一类是大部分普通产品,如医用非灭菌口罩,制造商做自我符合声明,加贴CE标志;另一类是少部分风险程度相对较高的产品,如医用灭菌口罩和个人防护口罩,需要经过欧盟授权的第三方公告机构认证产品的符合性,通过后才能加贴CE标志。
两类加贴CE标志的流程如下
二、欧盟授权代表
为更好的监管进入欧盟市场的产品,实现产品的溯源以及保护欧盟消费者权益,欧盟对于境外的生产商实行欧盟授权代表(European Authorised Representative, EAR)制度。所以我国的医疗器械生产商,需要在欧盟境内指定一位欧盟授权代表,来履行欧盟相关的指令和法律所要求的特定职责,代替生产商在欧盟进行相关活动。例如在欧盟的主管部门登记产品的自我声明、产品的变更和报告不良事件等。合格的EAR,不仅需要对医疗器械标准法规熟悉,还要有过硬的技术能力和良好的公关能力。国内生产商可根据自身实际情况,自主选择符合要求的欧盟成员国境内自然人或法人成为EAR,双方签订协议,并规定各自承担的职责。