2020年7月16日国家药品监督管理局医疗器械技术审评中心(以下简称器审中心)发布通知《关于征集参与编制重组人胶原蛋白质量评价技术审查等14项指导原则工作相关企业及单位信息》,旨在指导申请人对重组人胶原蛋白等相关产品注册申报资料的准备及撰写,进一步做好产品的技术审评工作。器审中心启动重组人胶原蛋白质量评价技术审查等14项指导原则的编制工作,希望有上述产品研发、生产或已有获批产品的境内、外企业及其他相关单位积极参与配合指导原则制修订工作。具体有哪些指导原则呢,快随小编来看看吧!
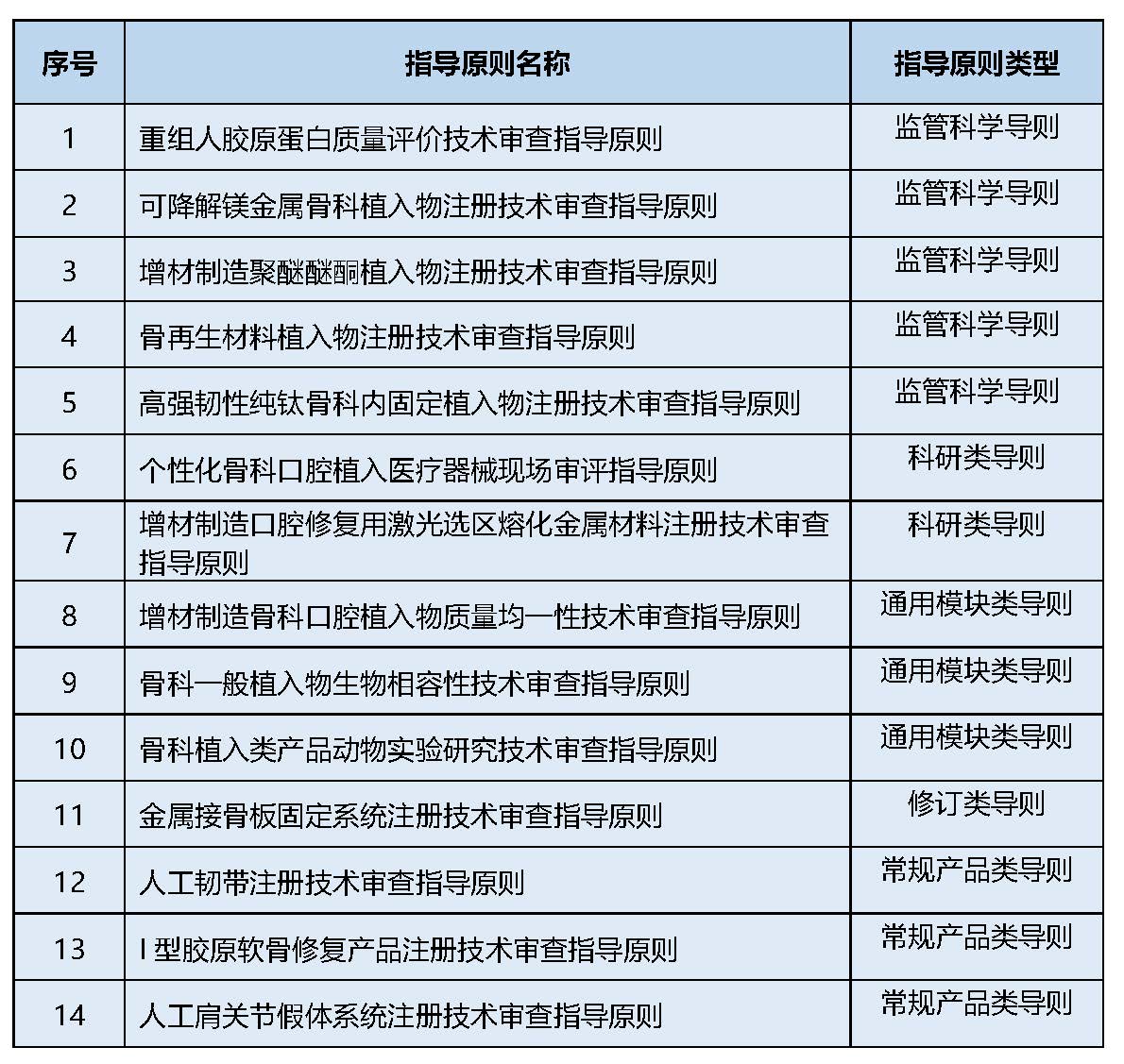
心动不如行动!有意向参与工作的相关单位请填写信息征集表,并于2020年8月5日前统一以电子版形式报送器审中心。
联系人:高进涛,金乐
电 话: 010-86452813, 010-86452802
电子邮箱:gaojt@cmde.org.cn,jinle@cmde.org.cn
附件下载:信息征集表
【原文来源】国家药品监督管理局医疗器械技术审评中心
【全文整理】苏州大学卫生与环境技术研究所
【声明】如果您认为我们的内容或来源标注与原文不符,请告知我们,我们将与您积极协商解决。谢谢大家的关注!