2020年7月20日国家药品监督管理局发布《关于发布笑气吸入镇静镇痛装置注册技术审查指导原则的通告》(2020年 第49号),旨在指导注册申请人对笑气吸入镇静镇痛装置注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。
适用于笑气吸入镇静镇痛装置,按照《医疗器械分类目录》,笑气吸入镇静镇痛装置的管理类别为Ⅲ类。
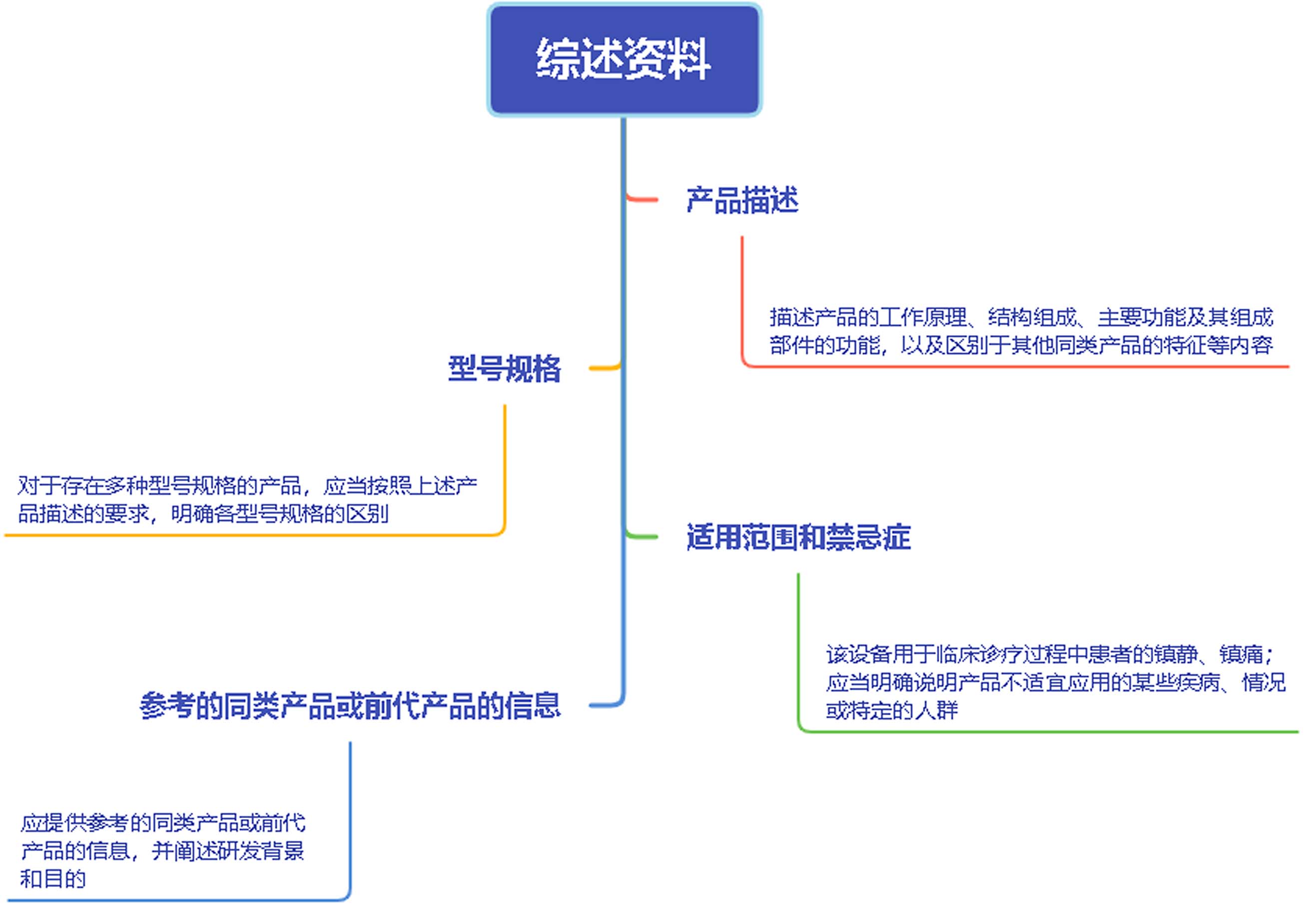
二、综述资料
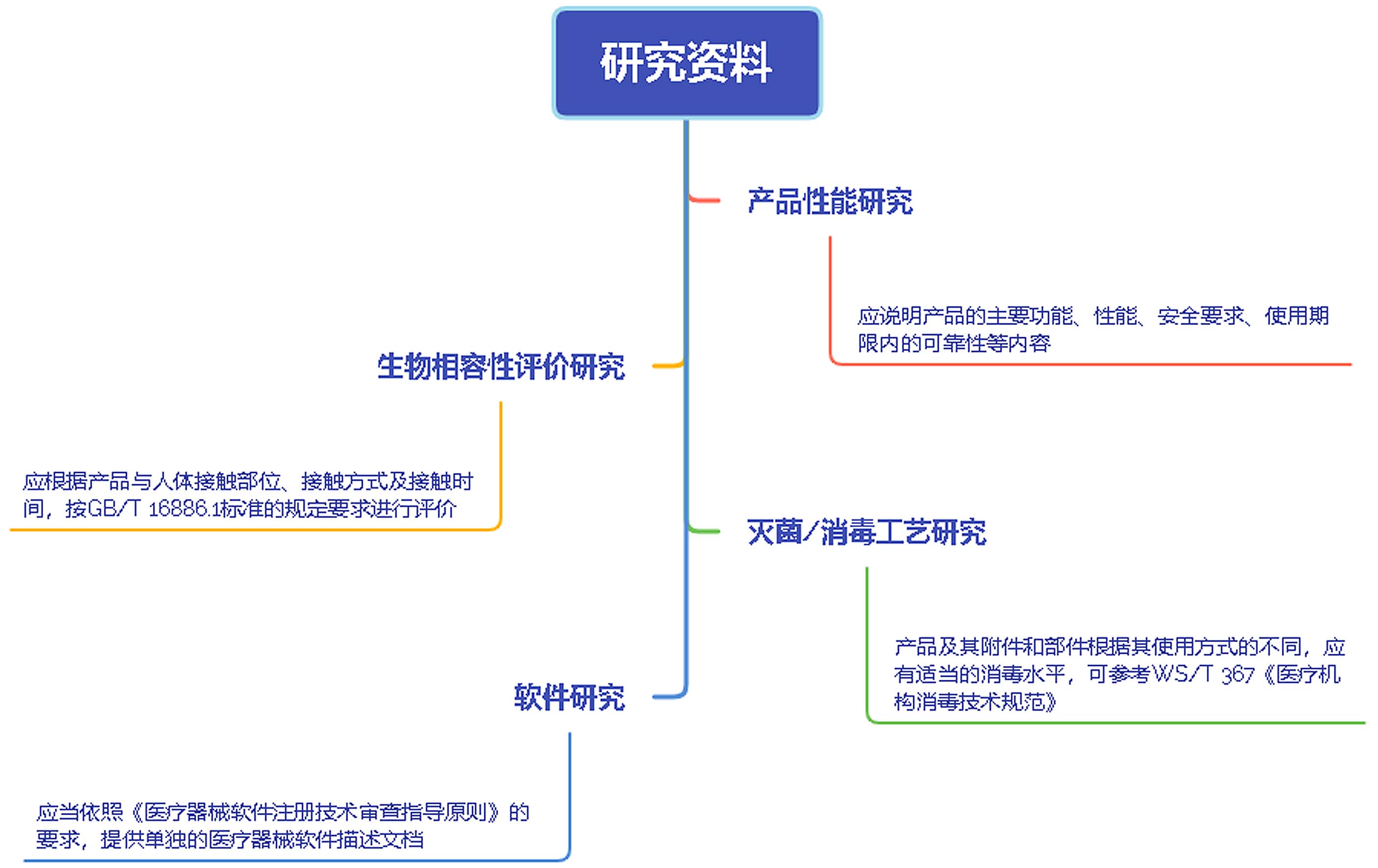
三、研究资料
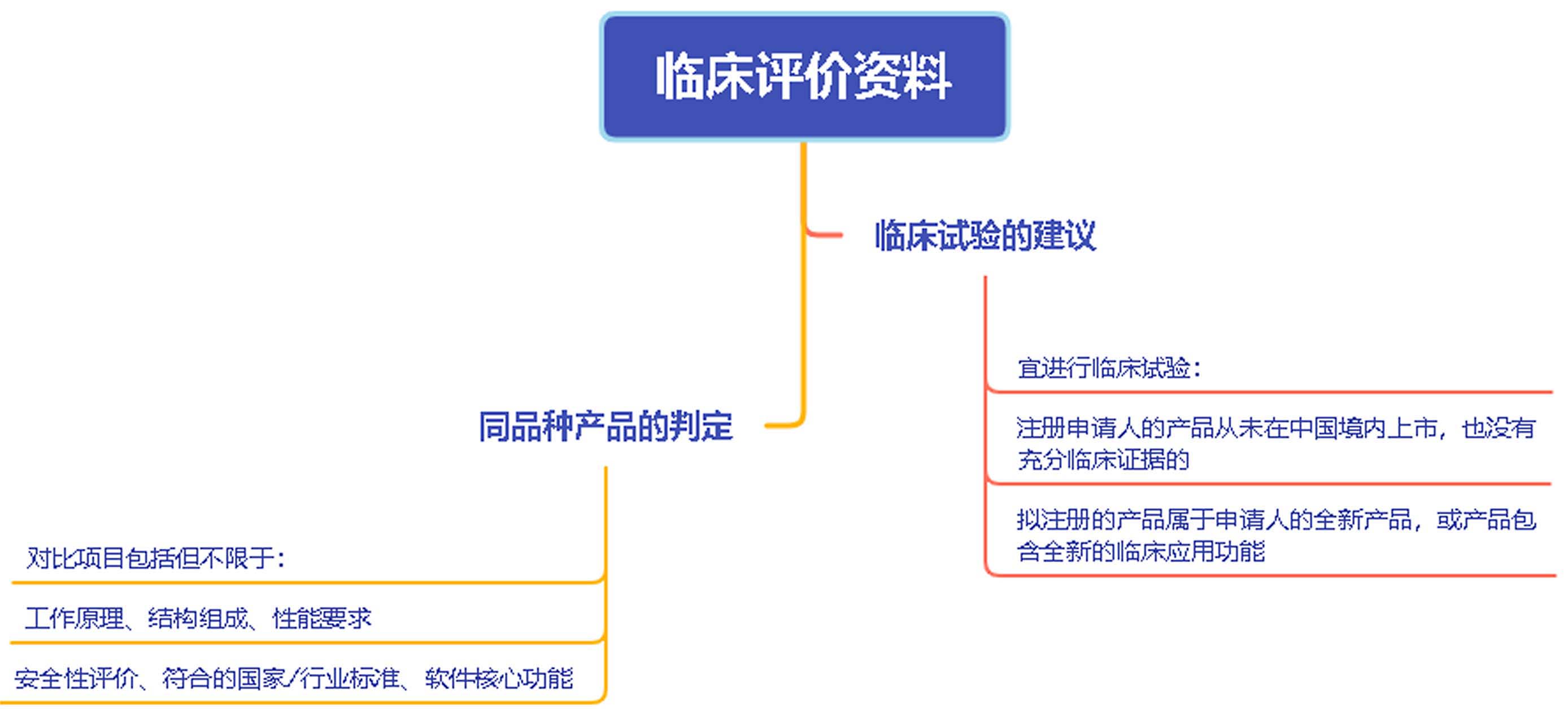
五、临床评价资料
六、产品风险分析资料
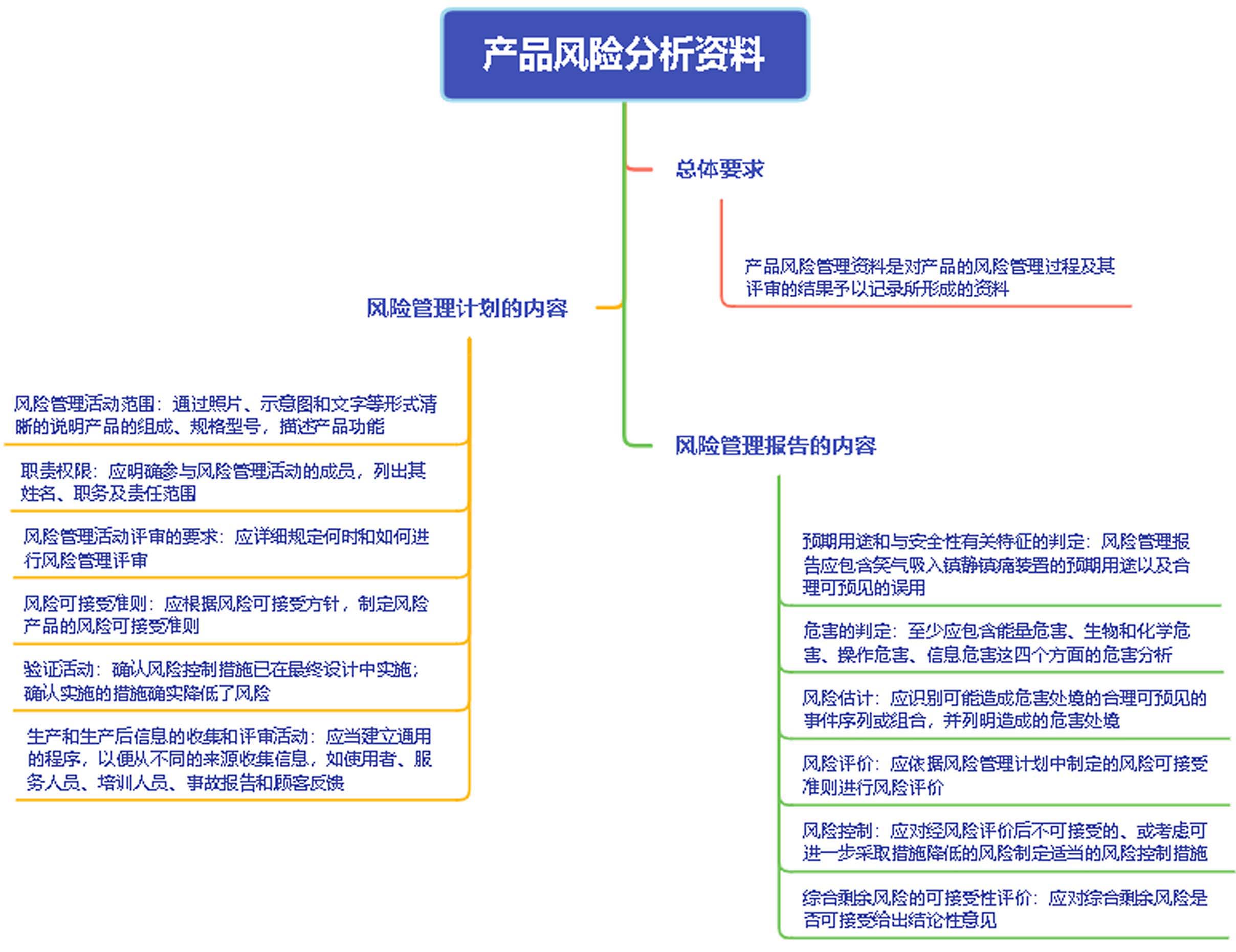
七、产品技术要求
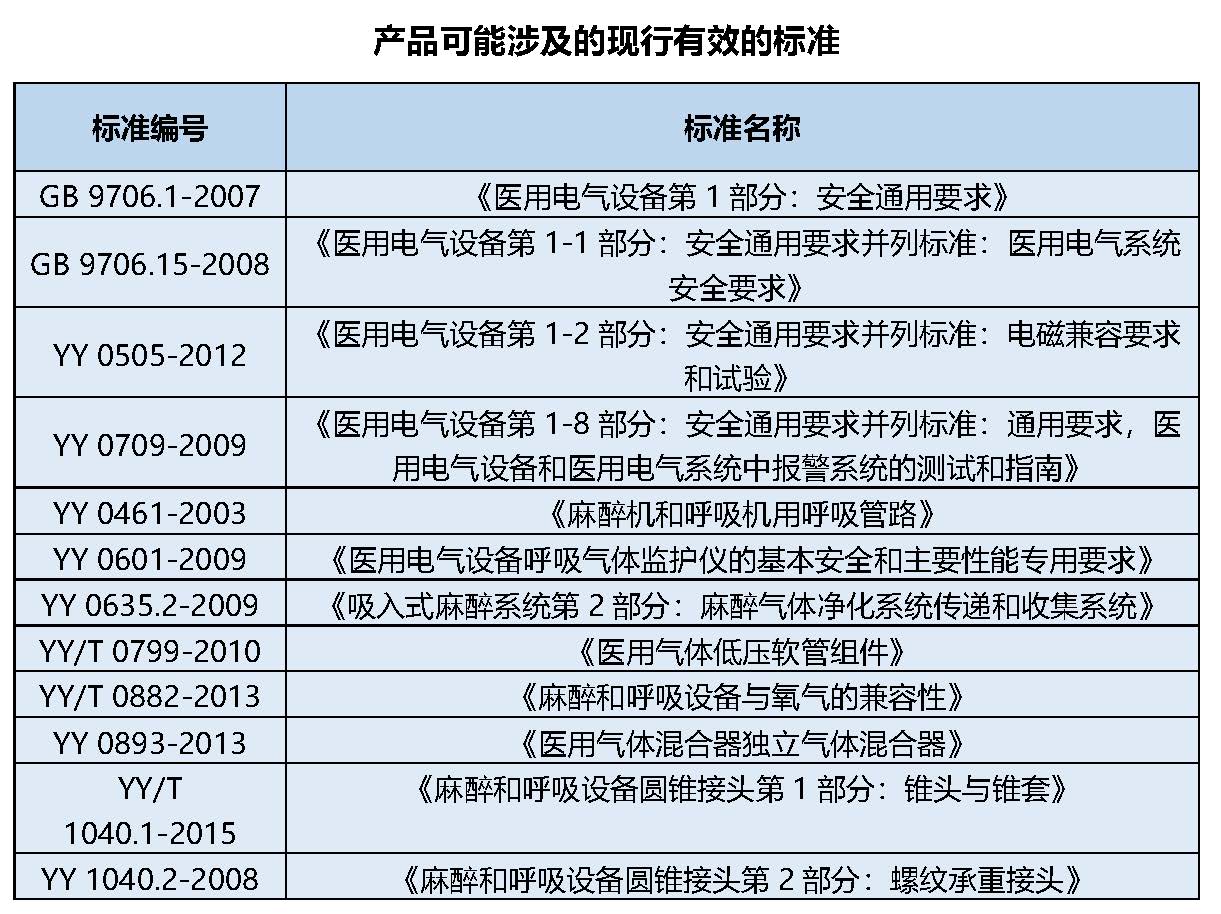
1、相关标准
申请人应根据申报注册产品的实际情况,确定标准的适用性。对不适用的标准,应在研究资料部分做出说明。
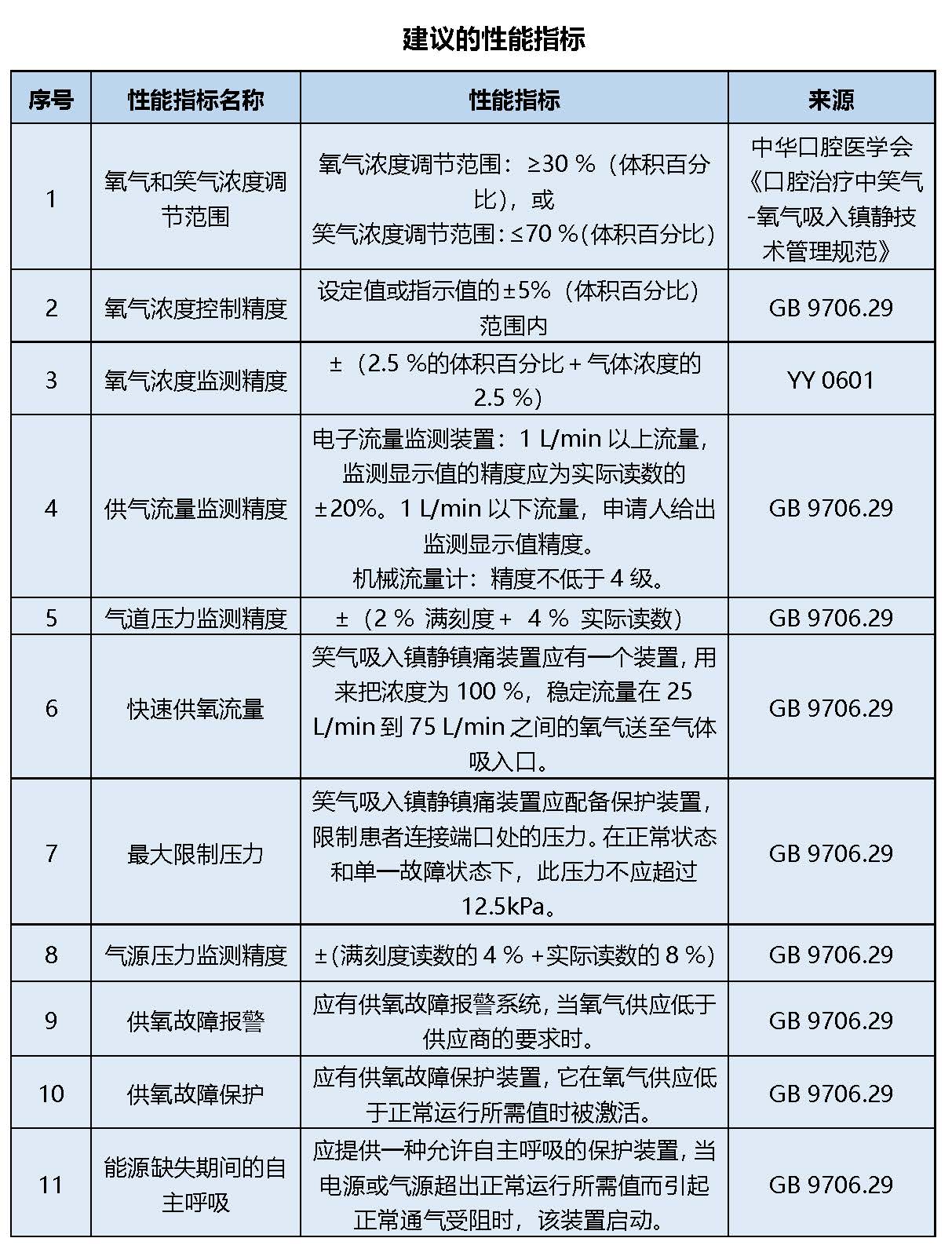
2、性能指标
本部分给出至少需要考虑的产品主要技术指标及参数要求,部分性能指标给出了明确的定量要求,其他性能指标因考虑不同产品的差异,未规定限值,需结合自身产品特点自行量化。
1、不同工作原理的产品应划分为不同的注册单元;
2、技术原理相同,但产品适用范围不同的,或主要结构、组成的不同对安全有效性有影响的,或性能差异较大的,划分为不同注册单元;
3、与产品配合/组合使用的无源类耗材原则上与产品划分为不同的注册单元。
1、产品说明书和标签文字内容应当使用中文,也可以附加其他文种,但应当以中文表达为准;
2、应当提供完整的使用说明书,其内容包含申报范围内所有型号规格的产品,以及所有的组成部分;
3、使用说明书应当符合相关标准的要求。
原文链接:http://www.nmpa.gov.cn/WS04/CL2138/378758.html
【原文来源】国家药品监督管理局
【全文整理】苏州大学卫生与环境技术研究所
【声明】如果您认为我们的内容或来源标注与原文不符,请告知我们,我们将与您积极协商解决。谢谢大家的关注!