2020年7月14日国家药品监督管理局医疗器械技术审评中心发布通知,关于公开征求《电子上消化道内窥镜注册技术审查指导原则(征求意见稿)》意见,旨在为技术审评部门审评注册申报资料提供参考,同时也指导申请人对电子上消化道内窥镜(以下简称内窥镜)注册申报资料的准备及撰写。下面就让小编带您具体了解指导原则的详细内容吧!
适用于电子上消化道内窥镜产品(不包括电子十二指肠内窥镜),其他软性电子内窥镜可参考该指导原则中适用的内容。
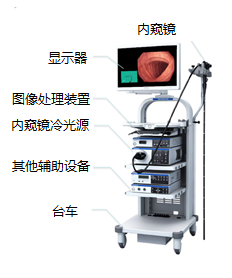
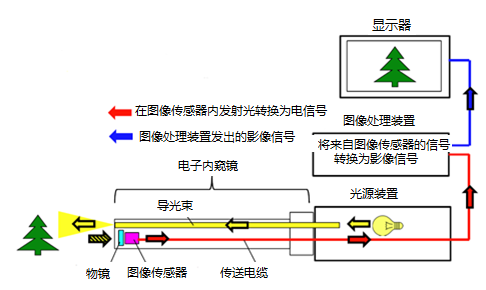
电子上消化道内窥镜成像系统一般包括内窥镜、图像处理装置、内窥镜冷光源、显示器和其他辅助设备。内窥镜成像系统和流程图如图所示:
电子上消化道内窥镜成像系统
内窥镜成像流程图
根据《医疗器械注册管理办法》第七十四条规定,医疗器械注册单元原则上以产品的技术原理、结构组成、性能指标和适用范围为划分依据。
►产品名称
产品名称一般由一个核心词和不超过三个特征词组成,电子上消化道内窥镜核心词为内窥镜,特征词分别为电子和观察部位。
►适用范围
电子上消化道内窥镜一般在医院内镜室使用,通过口腔或鼻腔进入人体消化道,对预期区域或部位进行照明并于体外成像以供观察和诊查,结合手术器械可进行内镜手术和治疗。
►结构和组成
电子上消化道内窥镜为软性电子内窥镜,一般为直视型,镜体由头端部、弯曲部、插入部、操作部及连接部组成。
►医疗器械安全有效基本要求清单
申请人应明确清单中各条款的适用性,对于不适用的条款,应详细说明理由。对于适用的条款,证明符合性采用的方法和为符合性提供客观证据的文件由申请人根据实际情况进行填写。
►综述资料
►研究资料
研究资料中性能、功能指标的确定依据应明确具体,应说明是产品什么特点,何种临床需求。
按照GB/T 16886.1标准的要求,对与患者接触部分的材料的生物相容性进行评价研究建议至少考虑以下方面的要求:细胞毒性、致敏、皮内反应。
应明确消毒工艺,提供消毒工艺确定依据,证明消毒工艺可达到高水平消毒的效果。可参考《可重复使用医疗器械再处理说明和确认方法注册技术审查指导原则》的要求提交完整的再处理说明确认方案和报告。
可从使用频率、消毒灭菌以及老化等方面对使用期限影响因素进行综合分析评估。
申请人应提交环境试验研究资料和包装研究资料,对包装和产品进行模拟试验。
内窥镜如含有软件组件,应提交软件相关的资料,包括验证、确认报告。
►临床评价
►产品的主要风险
►产品技术要求
应按照《医疗器械产品技术要求编写指导原则》编写产品技术要求,通常应包括光学性能、机械性能、材料、电气安全、电磁兼容等指标。
►检验报告
检验产品典型性:同一注册单元选择结构最复杂、功能最多、技术指标最高的型号进行检验。
►说明书和标签
说明书和标签应符合《医疗器械说明书和标签管理规定》、GB9706.1、GB9706.19以及YY0505中有关说明书和标签的要求。
【原文来源】国家药品监督管理局医疗器械技术审评中心
【全文整理】苏州大学卫生与环境技术研究所
【声明】如果您认为我们的内容或来源标注与原文不符,请告知我们,我们将与您积极协商解决。谢谢大家的关注!