2020年09月29日,国家药品监督管理局医疗器械技术审评中心发布关于公开征求《一次性使用注射笔配套用针注册审查技术指导原则(征求意见稿)》意见的通知,旨在帮助和指导申请人对一次性使用注射笔配套用针(以下简称注射笔配套用针)产品的注册申报资料进行准备,以满足技术审评的基本要求。为了更好的帮助您快速了解内容,为您梳理出重点内容,供您阅览!
 敲黑板,划重点
敲黑板,划重点
一、适用范围
适用于作为医疗器械管理的注射笔配套用针产品注册申报资料的准备及产品技术审评的参考。
二、注册申报资料要求
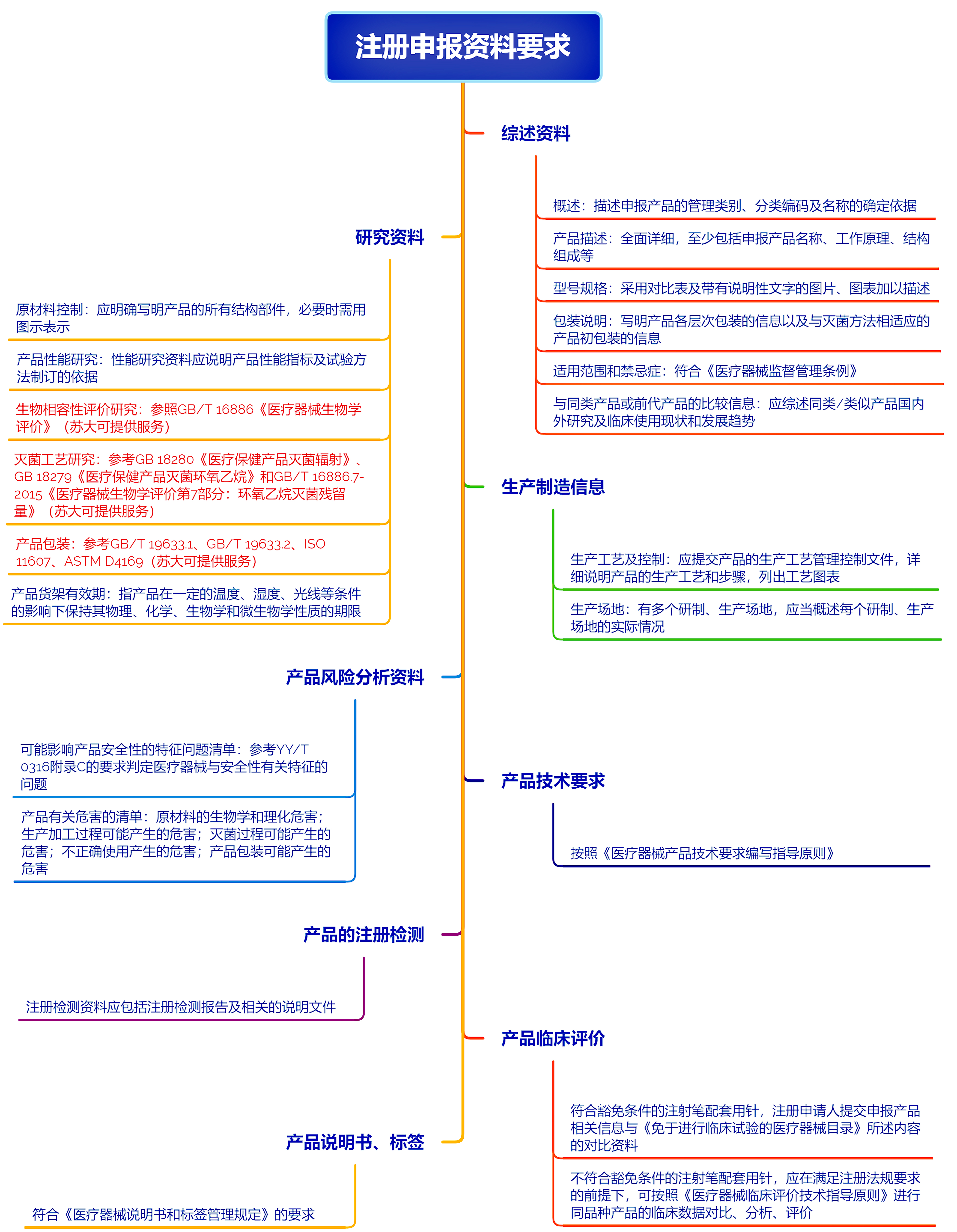
原文链接:https://www.cmde.org.cn/CL0004/21720.html
【原文来源】国家药品监督管理局医疗器械技术审评中心
【全文整理】苏州大学卫生与环境技术研究所
【声明】如果您认为我们的内容或来源标注与原文不符,请告知我们,我们将与您积极协商解决。谢谢大家的关注。
下载附件1-2