摘要:10月NMPA、CMDE发布的法规通告汇总
合集:#法规汇总
公告
依据原国家食品药品监督管理总局《医疗器械优先审批程序》(总局公告2016年168号),我中心对申请优先审批的医疗器械注册申请进行了审核。下述项目符合优先审批情形,拟定予以优先审批,现予以公示。

公示时间:2023年10月23日至2023年10月30日
公示期内,任何单位和个人有异议的,可以填写医疗器械优先审批项目异议表,书面提交至我中心综合业务部。
联 系 人:张欣
电话:010-86452928
电子邮箱:gcdivision@cmde.org.cn
地址:北京市海淀区气象路50号院1号楼
原文链接:医疗器械优先审批申请审核结果公示(2023年第8号) (cmde.org.cn)
为做好医疗器械注册受理前技术问题咨询工作,指导行政相对人安排咨询时间,保证咨询工作质量,现就近期咨询工作安排通告如下:
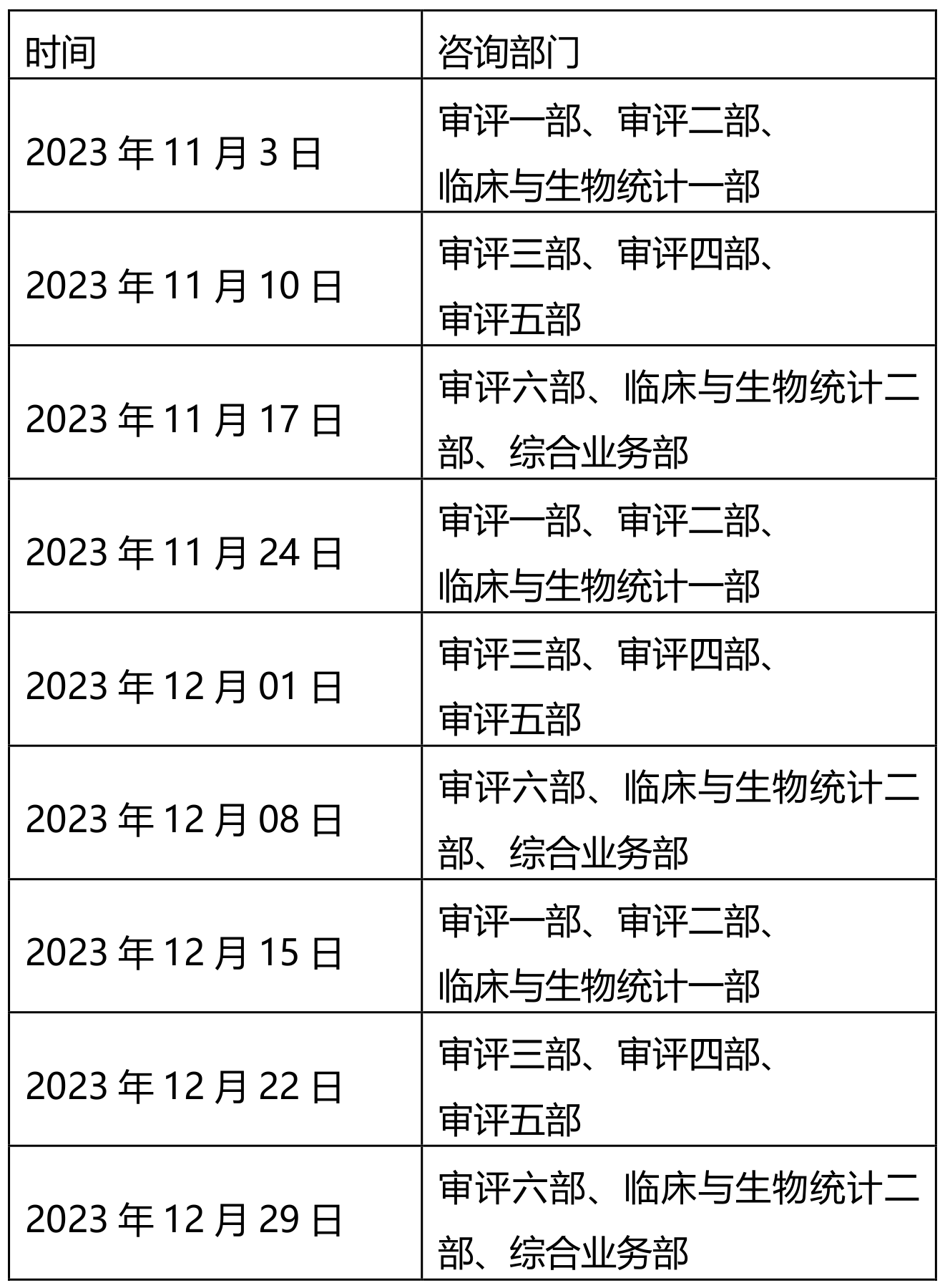
注:受理前咨询工作暂时采用视频会议方式进行,申请人预约成功后请等待电话通知。请申请人按照我中心2022年10月16日发布的《关于医疗器械受理前技术问题咨询工作安排调整的通告》(2022年第37号)的要求申请和办理,各受理前技术问题咨询参与单位咨询时间安排同器审中心,但不受轮值部门限制。
原文链接:关于2023年11月~12月医疗器械注册受理前技术问题咨询工作安排的通告(2023年第37号) (cmde.org.cn)
为进一步优化医疗器械标准体系,国家药监局决定废止YY 0569-2011《Ⅱ级生物安全柜》和YY/T 0687-2008《外科器械 非切割铰接器械 通用技术条件》2项医疗器械行业标准,现予以公布(见附件)。
特此公告。
《中华人民共和国药典》(2020年版)第一增补本已编制完成,现予发布(目录见附件),自2024年3月12日起施行。
特此公告。
原文链接:国家药监局 国家卫生健康委关于发布实施《中华人民共和国药典》(2020年版)第一增补本的公告(2023年第126号) (nmpa.gov.cn)
征集
1. 【CMDE】关于公开征求《电动摄影平床注册审查指导原则(征求意见稿)》等54项第二类医疗器械注册审查指导原则意见的通知 – 2023.10.25
各有关单位:
根据国家药品监督管理局医疗器械注册审查指导原则项目计划的有关要求,我中心组织编制了《电动摄影平床注册审查指导原则(征求意见稿)》等54项第二类指导原则(附件1),现已形成征求意见稿,即日起在网上公开征求意见。如有意见和建议,请填写意见反馈表(附件2),并于2023年11月23日前反馈至相应的联系人(附件3)。
原文链接:关于公开征求《电动摄影平床注册审查指导原则(征求意见稿)》等54项第二类医疗器械注册审查指导原则意见的通知 (cmde.org.cn)
2. 【CMDE】关于公开征求《牙科种植体(系统)注册审查指导原则(2023年修订)》等两项医疗器械注册审查指导原则意见的通知 - 2023.10.23
各有关单位:
根据国家药品监督管理局2023年度医疗器械注册审查指导原则制修订计划的有关要求,我中心组织编制了《牙科种植体(系统)注册审查指导原则(2023年修订)》等两项医疗器械注册审查指导原则,经调研、讨论,现已形成征求意见稿(附件1),即日起在网上公开征求意见。
如有意见和建议,请填写意见反馈表(附件2),以电子邮件的形式于2023年11月18日前反馈至我中心相应联系人。邮件主题及文件名称请以“《XX注册审查指导原则(征求意见稿)》意见反馈+反馈单位名称”格式命名。
联系人:金乐
联系电话:010-86452802
电子邮箱:jinle@cmde.org.cn
原文链接:关于公开征求《牙科种植体(系统)注册审查指导原则(2023年修订)》等两项医疗器械注册审查指导原则意见的通知 (cmde.org.cn)
3. 【CMDE】关于公开征求《椎间融合器注册审查指导原则(2023年修订)》等四项医疗器械注册审查指导原则意见的通知 – 2023.10.23
各有关单位:
根据国家药品监督管理局2023年度医疗器械注册审查指导原则制修订计划的有关要求,我中心组织编制了《椎间融合器注册审查指导原则(2023年修订)》等四项医疗器械注册审查指导原则,经调研、讨论,现已形成征求意见稿(附件1~4),即日起在网上公开征求意见。
如有意见和建议,请填写意见反馈表(附件5),以电子邮件的形式于2023年11月18日前反馈至我中心相应联系人。邮件主题及文件名称请以“《XX注册审查指导原则(征求意见稿)》意见反馈+反馈单位名称”格式命名
原文链接:关于公开征求《椎间融合器注册审查指导原则(2023年修订)》等四项医疗器械注册审查指导原则意见的通知 (cmde.org.cn)
4.【NMPA】公开征求《医疗机构临床急需医疗器械临时进口使用管理要求(征求意见稿)》意见 – 2023.10.18
为做好《医疗器械监督管理条例》配套文件修订工作,国家药监局起草了《医疗机构临床急需医疗器械临时进口使用管理要求(征求意见稿)》等文件,现向社会公开征求意见。请于2023年11月15日前,将有关意见通过电子邮件方式反馈至ylqxzc@nmpa.gov.cn,邮件标题注明“急需进口使用意见”。
原文链接:国家药监局综合司公开征求《医疗机构临床急需医疗器械临时进口使用管理要求(征求意见稿)》意见 (nmpa.gov.cn)
各有关单位及个人:
按照国家药品监督管理局要求,为进一步完善医疗器械分类管理制度体系、规范医疗器械产品类别判定,国家药品监督管理局医疗器械标准管理中心起草了《医疗器械分类规则(修订草案征求意见稿)》(附件1)及修订说明(附件2),现公开征求意见。
若有意见或建议,请填写征求意见表(附件3),于2023年11月9日前发送至邮箱wys-xbs@nifdc.org.cn。邮件主题及附件名称请注明“《医疗器械分类规则》征求意见表+反馈单位名称或个人姓名”。
联系人及联系方式:温莉茵,010-53852617。
原文链接:关于征求《医疗器械分类规则(修订草案征求意见稿)》意见的通知 (nifdc.org.cn)



