一、公告
1.医疗器械优先审批申请审核结果公示(2022年第3号)
依据原国家食品药品监督管理总局《医疗器械优先审批程序》(总局公告2016年168号),我中心对申请优先审批的医疗器械注册申请进行了审核。下述项目符合优先审批情形,拟定予以优先审批,现予以公示。
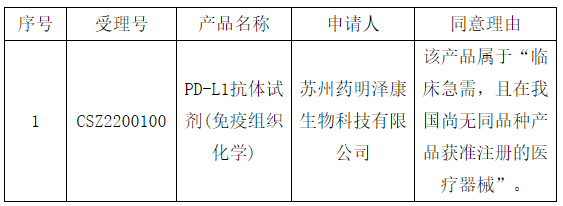
原文链接:https://www.nmpa.gov.cn/xxgk/ggtg/qtggtg/20220324100322197.html
2.创新医疗器械特别审查申请审查结果公示(2022年第4号)
依据国家药品监督管理局《创新医疗器械特别审查程序》(国家药监局2018年第83号公告)要求,创新医疗器械审查办公室组织有关专家对创新医疗器械特别审查申请进行了审查,拟同意7项首次申请项目进入特别审查程序,1项重新提出申请的创新医疗器械仍按照程序实施审查,现予以公示。
原文链接:https://www.nmpa.gov.cn/xxgk/ggtg/qtggtg/20220323100535112.html
3.国家药监局器审中心发布《医疗器械分类目录》子目录11、12、13、14、15、17、22相关产品临床评价推荐路径(2022年第20号)
为进一步指导注册申请人确定具体产品的临床评价路径,器审中心按照《医疗器械监督管理条例》的有关规定,根据《决策是否开展医疗器械临床试验技术指导原则》等规范要求,基于目前的审评经验以及《医疗器械分类目录》中的子目录11“医疗器械消毒灭菌器械”、12“有源植入器械”、13“无源植入器械”、14“注输、护理和防护器械”、15“患者承载器械”、17“口腔科器械”、22“临床检验器械”的产品描述、预期用途和品名举例,提出具体产品临床评价的推荐路径。
原文链接:https://www.nmpa.gov.cn/xxgk/ggtg/qtggtg/20220324101855146.html
4.国家药监局批准注册212个医疗器械产品公告(2022年4月)(2022年第38号)
2022年4月,国家药品监督管理局共批准注册医疗器械产品212个。其中,境内第三类医疗器械产品154个,进口第三类医疗器械产品35个,进口第二类医疗器械产品20个,港澳台医疗器械产品3个(具体产品见附件)。
原文链接:https://www.nmpa.gov.cn/xxgk/ggtg/ylqxpzhzhcchpgg/20220516154527116.html
5.国家药监局发布YY 0307-2022《激光治疗设备 掺钕钇铝石榴石激光治疗机》等55项医疗器械行业标准及2项医疗器械行业标准修改单(2022年第39号)
YY 0307-2022《激光治疗设备 掺钕钇铝石榴石激光治疗机》等55项医疗器械行业标准及2项医疗器械行业标准修改单已经审定通过,现予以公布。
原文链接:https://www.nmpa.gov.cn/xxgk/ggtg/qtggtg/20220324101855146.html
二、新发布技术指导原则
1.国家药监局器审中心发布肺结节CT图像辅助检测软件注册审查指导原则(2022年第21号)
为进一步规范肺结节CT图像辅助检测软件的管理,国家药监局器审中心组织制定了《肺结节CT图像辅助检测软件注册审查指导原则》,现予发布。
原文链接:https://www.cmde.org.cn/xwdt/zxyw/20220526102356105.html
【全文整理】苏大卫环