一、公告
1.【CMDE】发布《医疗器械分类目录》子目录02、03、05、06、16、18、20相关产品临床评价推荐路径的通告(2022年第24号)
器审中心按照《医疗器械监督管理条例》的有关规定,根据《决策是否开展医疗器械临床试验技术指导原则》等规范要求,基于目前的审评经验以及《医疗器械分类目录》中的子目录02“无源手术器械”、03“神经和心血管手术器械”、 05“放射治疗器械”、06“医用成像器械”、16“眼科器械”、18“妇产科、辅助生殖和避孕器械”、20“中医器械”的产品描述、预期用途和品名举例,提出具体产品临床评价的推荐路径。特此通告。
原文链接:
https://www.cmde.org.cn/xwdt/zxyw/20220616154413150.html
2.【CMDE】发布关于2022年7月~8月医疗器械注册受理前技术问题咨询工作安排的通告(2022年第25号)
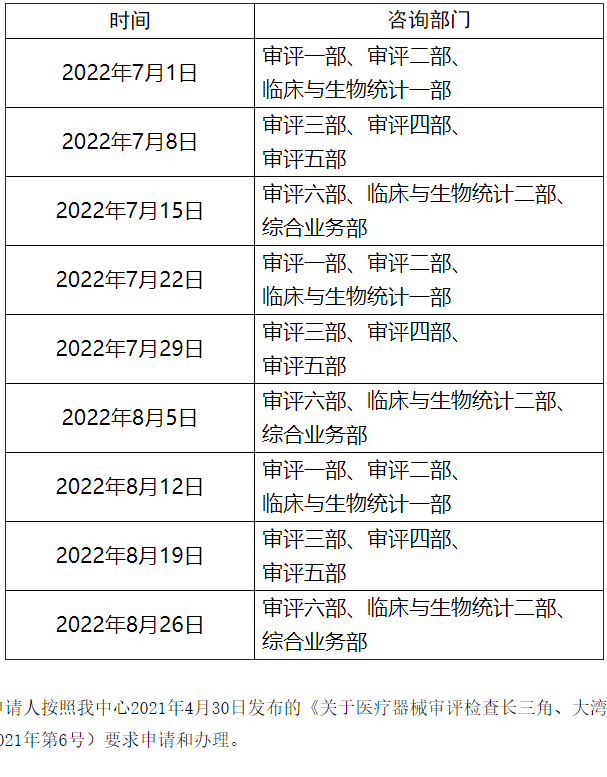
为做好医疗器械注册受理前技术问题咨询工作,指导行政相对人安排咨询时间,保证咨询工作质量,现就近期咨询工作安排通告如下:
注:按照疫情防控要求,受理前咨询工作采用视频会议方式进行,申请人预约成功后请等待电话通知。
原文链接:
https://www.cmde.org.cn/xwdt/zxyw/20220622142810178.html
3.【CMDE】发布2022年度医疗器械注册审查指导原则编制计划的通告(2022年第26号)
为进一步加强医疗器械注册审查指导原则在注册申报和技术审评工作中的指导作用,我中心组织拟订了医疗器械注册审查指导原则编制计划(详见附件),现予以发布。特此通告。
原文链接:https://www.cmde.org.cn/xwdt/zxyw/20220623140439147.html
4.国家药监局关于批准注册164个医疗器械产品公告(2022年5月)(2022年第46号)
2022年5月,国家药品监督管理局共批准注册医疗器械产品164个。其中,境内第三类医疗器械产品109个,进口第三类医疗器械产品23个,进口第二类医疗器械产品30个,港澳台医疗器械产品2个。
原文链接:
https://www.nmpa.gov.cn/xxgk/ggtg/ylqxpzhzhcchpgg/20220616160302154.html
5.国家药监局发布18项医疗器械行业标准的公告(2022年第52号)
YY/T 1833.1-2022《人工智能医疗器械 质量要求和评价 第1部分:术语》等
18项医疗器械行业标准已经审定通过,现予以公布。
原文链接:https://www.nmpa.gov.cn/xxgk/ggtg/qtggtg/20220706104425173.html
二、新发布技术指导原则
1.【CMDE】发布糖尿病视网膜病变眼底图像辅助诊断软件注册审查指导原则的通告(2022年第23号)
为进一步规范糖尿病视网膜病变眼底图像辅助诊断软件的管理,国家药监局器审中心组织制定了《糖尿病视网膜病变眼底图像辅助诊断软件注册审查指导原则》,现予发布。
原文链接:https://www.cmde.org.cn/xwdt/zxyw/20220602103048151.html
三、征求意见稿
1.【CMDE】征求免于进行临床评价医疗器械目录和免于临床试验体外诊断试剂目录意见
我中心启动了2022年度豁免目录的制修订工作,我中心形成了《建议新增和修订的免于临床评价医疗器械目录(2022年征求意见稿)》(见附件1),即日起在中心网站公开征求意见。请各有关单位于2022年8月8日前相关意见或建议发送至邮箱:huangyl@cmde.org.cn。
原文链接:
https://www.cmde.org.cn/xwdt/zxyw/20220705144811103.html
2.【CMDE】征求《血液透析浓缩物注册审查指导原则(征求意见稿)》等2项指导原则意见
我中心结合医疗器械注册法规、境内外注册申报产品的特点及申报现状,在总结技术审评实际情况,参考相关文献资料的基础上,对已经发布实施的血液透析浓缩物、血液透析器注册审查指导原则进行了修订,形成《血液透析浓缩物注册审查指导原则(征求意见稿)》、《血液透析器注册审查指导原则(征求意见稿)》,现公开征求意见。
原文链接:
https://www.cmde.org.cn/xwdt/zxyw/20220628111631119.html
3.【CMDE】征求《中医熏蒸治疗设备注册审查指导原则(征求意见稿)》等5项中医类医疗器械注册审查指导原则意见
根据国家药品监督管理局医疗器械注册审查指导原则项目计划的有关要求,我中心组织编制了《中医熏蒸治疗设备注册审查指导原则(征求意见稿)》等5个第二类指导原则(附件1),现已形成征求意见稿。如有意见和建议,请填写意见反馈表(附件2),并于2022年7月25日前反馈。
原文链接:
https://www.cmde.org.cn/xwdt/zxyw/20220623164120132.html
4.【CMDE】征求《药物涂层球囊扩张导管注册审查指导原则(征求意见稿)》意见
为进一步规范药物涂层球囊扩张导管的注册申报和技术审评,我中心组织起草了《药物涂层球囊扩张导管注册审查指导原则(征求意见稿)》,现公开征求意见。
原文链接:
https://www.cmde.org.cn/xwdt/zxyw/20220622141635108.html
【全文整理】苏大卫环