临床前动物试验是医疗器械临床试验伦理审批的必需项目,也是高风险器械注册审查中的重要内容。临床前动物试验通过将产品应用于动物模型来模拟临床使用,同时借助解剖学、影像学、临床病理学等手段,综合评价产品的安全性、有效性及性能,可用于证明创新概念,验证研发改进,评价定型产品,培训临床医生。相较生物相容性试验,临床前动物试验的动物模型与人体反应更为接近,能够模拟产品实际使用情况和预期用途的符合性,可为人体临床试验提供客观证据和辅助参考。
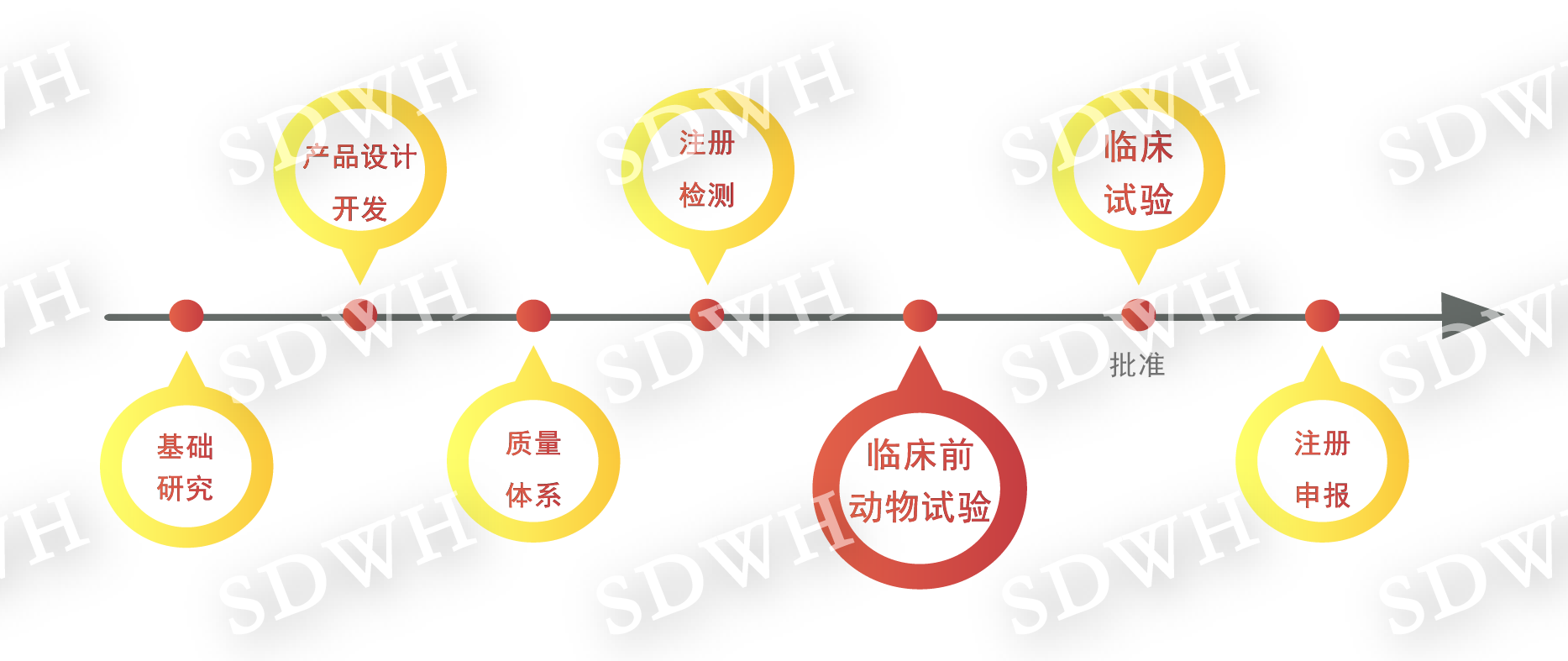
高风险医械产品上市流程
具体可参考国家药品监督管理局发布的《医疗器械动物试验研究技术审查指导原则 第一部分:决策原则》。
点击查看原文链接:https://www.cmde.org.cn/CL0112/19031.html
决策开展动物试验的流程图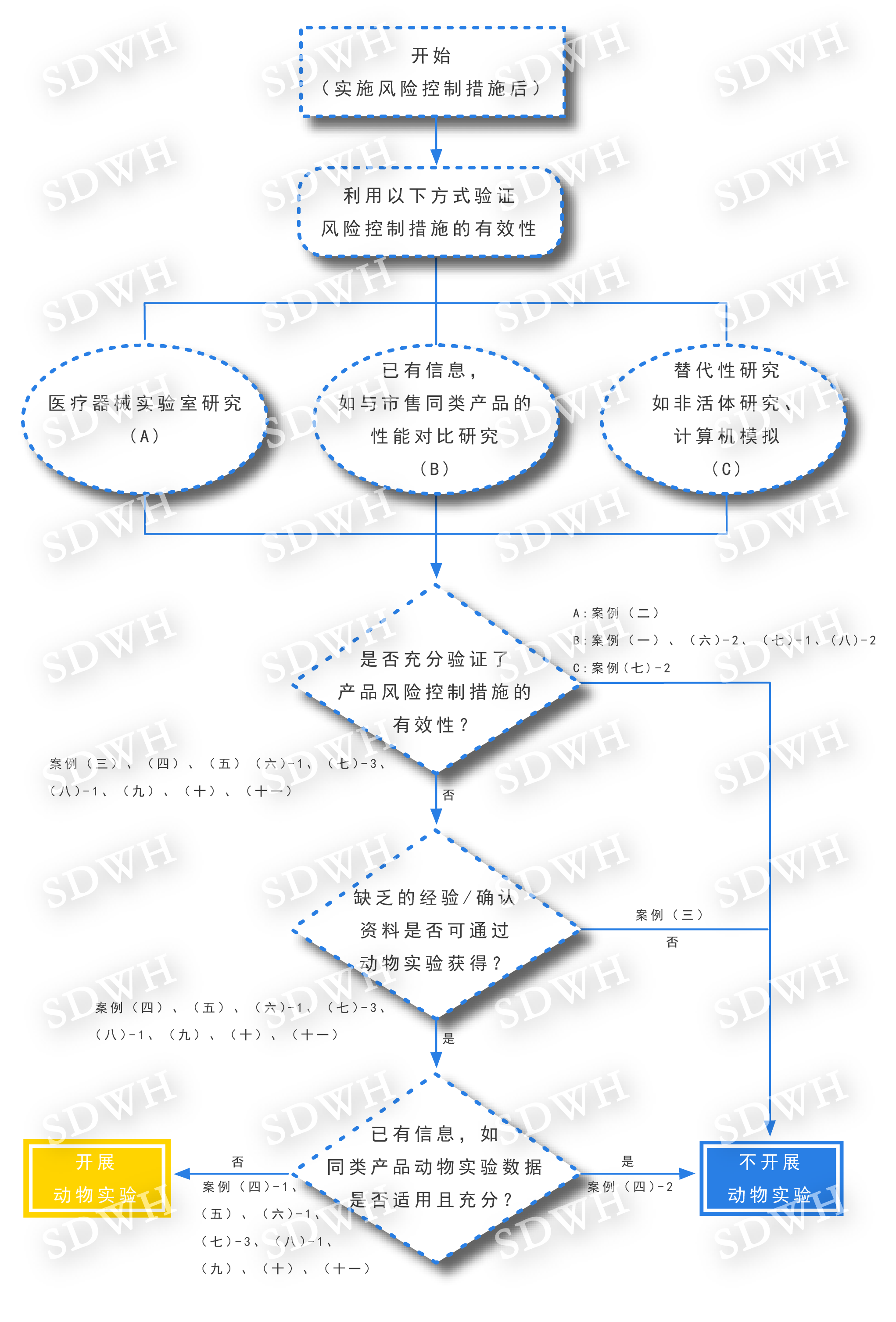
是否开展动物试验的决策案例
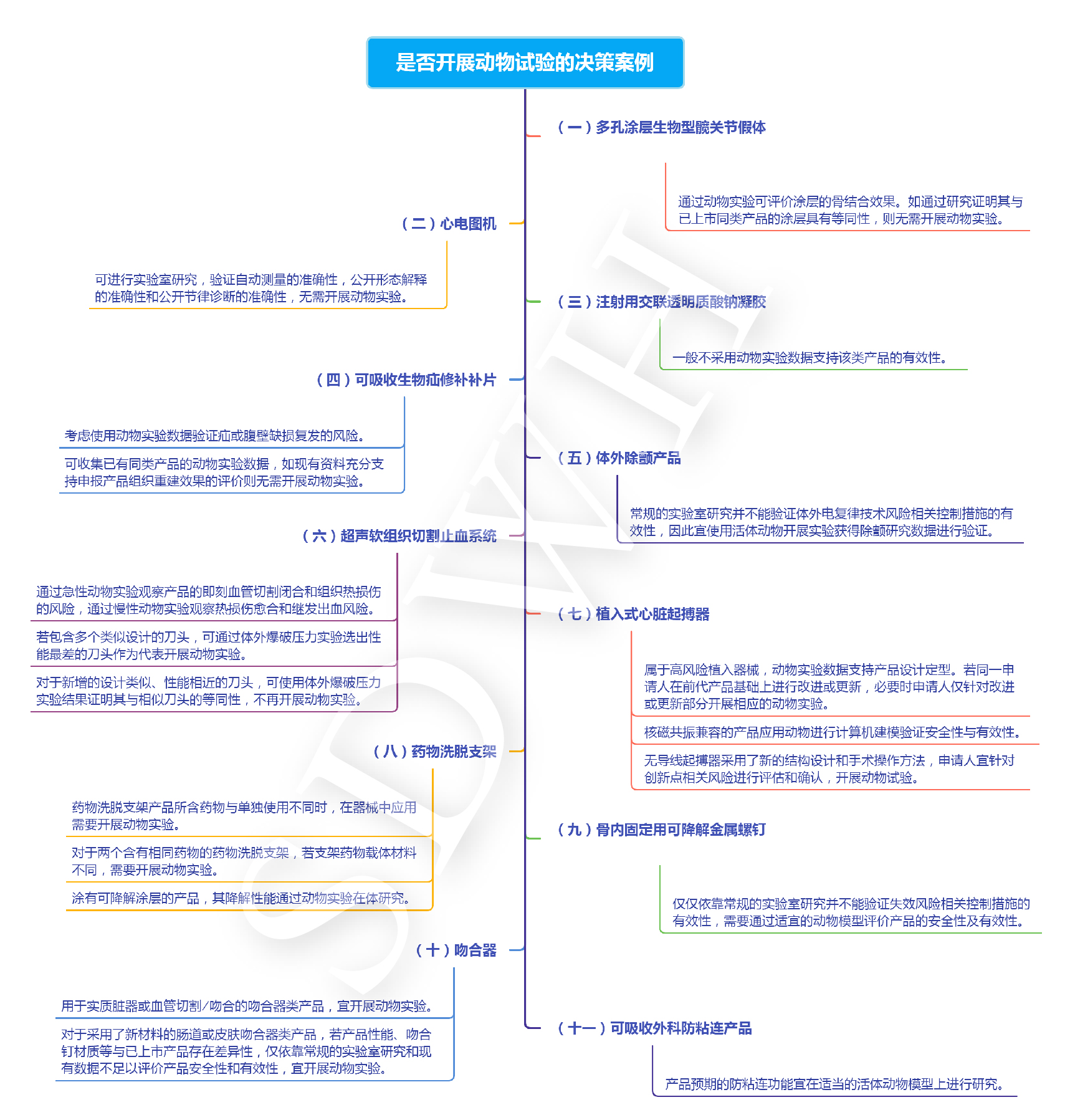
设计参考的通用原则
通用原则:可参考国家药品监督管理局发布的《医疗器械动物试验研究技术审查指导原则 第二部分:实验设计、实施质量保证》(征求意见稿)
点击查看原文链接:NMPA https://www.cmde.org.cn/CL0101/20038.html
FDA发布的《General Considerations for Animal Studies for Medical Devices Draft Guidance for Industry and Food and Drug Administration Staff》。
点击查看原文链接:FDA http://fda.maharashtra.gov.in/
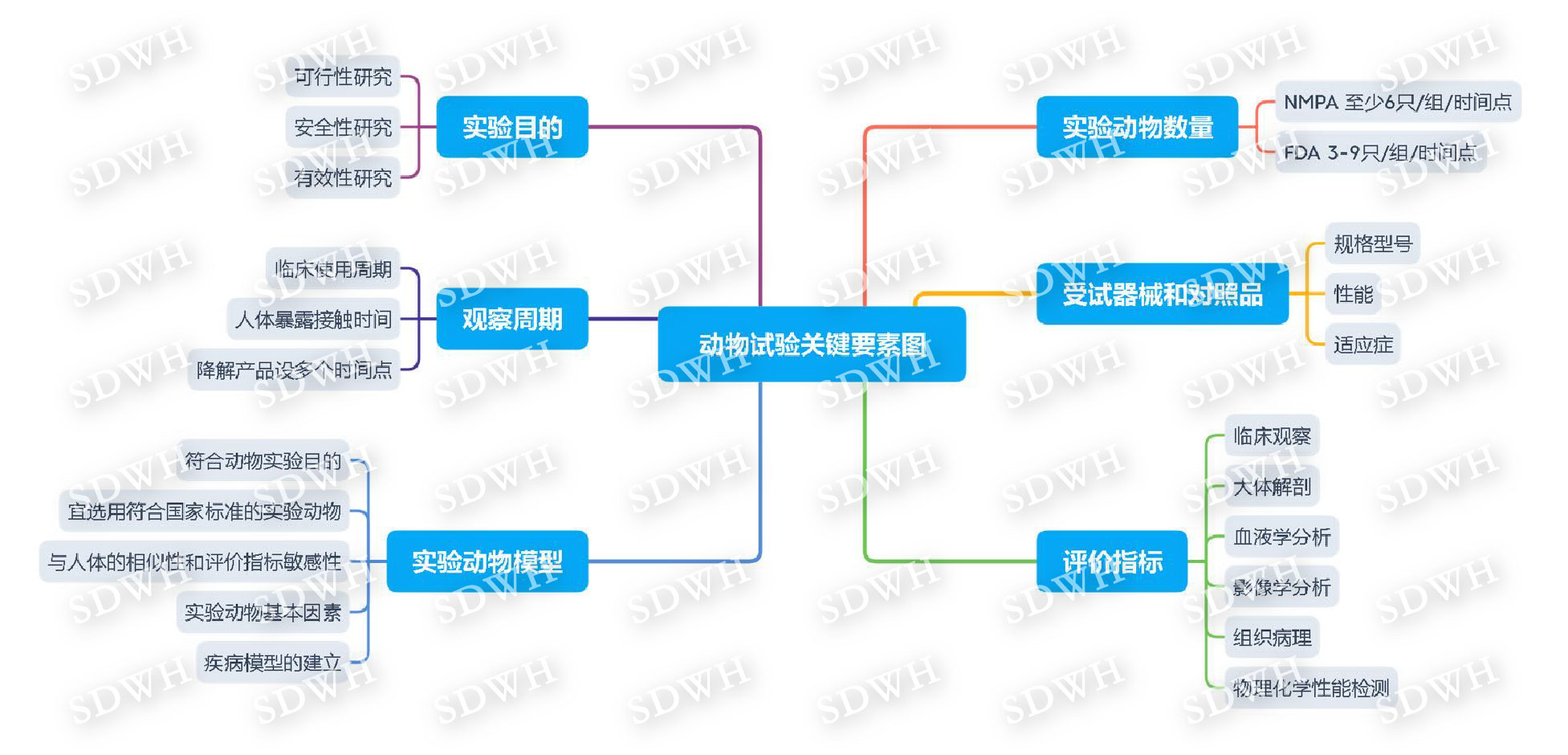
动物试验关键要素
2020年5月20日,医疗器械技术审评中心(以下简称“器审中心”)官方网站“分类目录指导原则”栏目正式上线。该栏目汇总了涉及医疗器械和体外诊断试剂的300余项已发布指导原则。小编已将其中提到需要考虑开展临床前动物试验的指导原则整理成表,以供您快速查阅!

扫码查看 已发布的涉及临床前动物试验的注册技术审评指导原则
我所作为第三方医疗器械检验检测机构深耕于医疗器械检测行业30余年,提供专业权威的医疗器械产品和原材料检测和评价服务。对于临床前动物试验检测,我所具备:
我所临床前动物试验项目经验:
超声骨刀、超声止血刀
骨板及髓内钉、骨科填充替代材料、软骨关节胶原蛋白、脑膜补片、透明质酸填充材料、鼻假体、输尿管支架
牙科种植体、牙科填充材料
骨固定系统
微球栓塞剂
防粘连剂、胰岛素输注器、烧伤敷料、皮肤补片
体外除颤器
内窥镜、显影标记物胶囊
【文章来源】国家药品监督管理局
【全文整理】苏州大学卫生与环境技术研究所
【声明】如果您认为我们的内容或来源标注与原文不符,请告知我们,我们将与您积极协商解决。谢谢大家的关注!