2020年05月29日,国家药品监督管理局医疗器械技术审评中心发布要闻《医疗器械注册审评项目智能化分配初见成效》。文中提到,截至2020年4月30日,eRPS系统累计接收各类注册申请事项22773件,通过线上途径提交19640件,占注册申报总量的86%,并持续稳定增长。这标示着医疗器械注册正式进入云时代啦,您足不出户就能办理医疗器械产品注册申请。小编为您整理了医疗器械注册电子申报的相关要点,快来看看吧。
一、医疗器械注册电子申报的适用范围
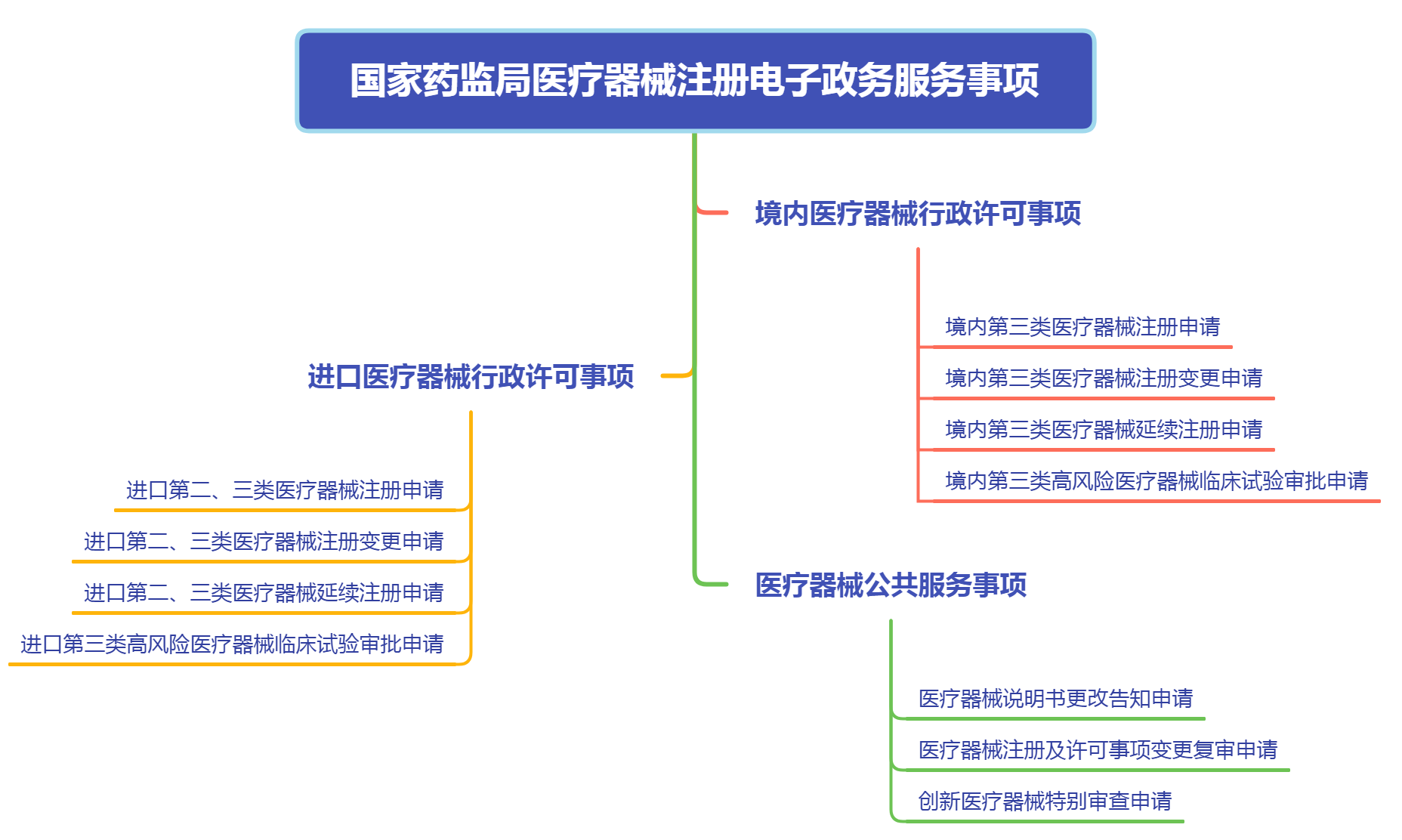
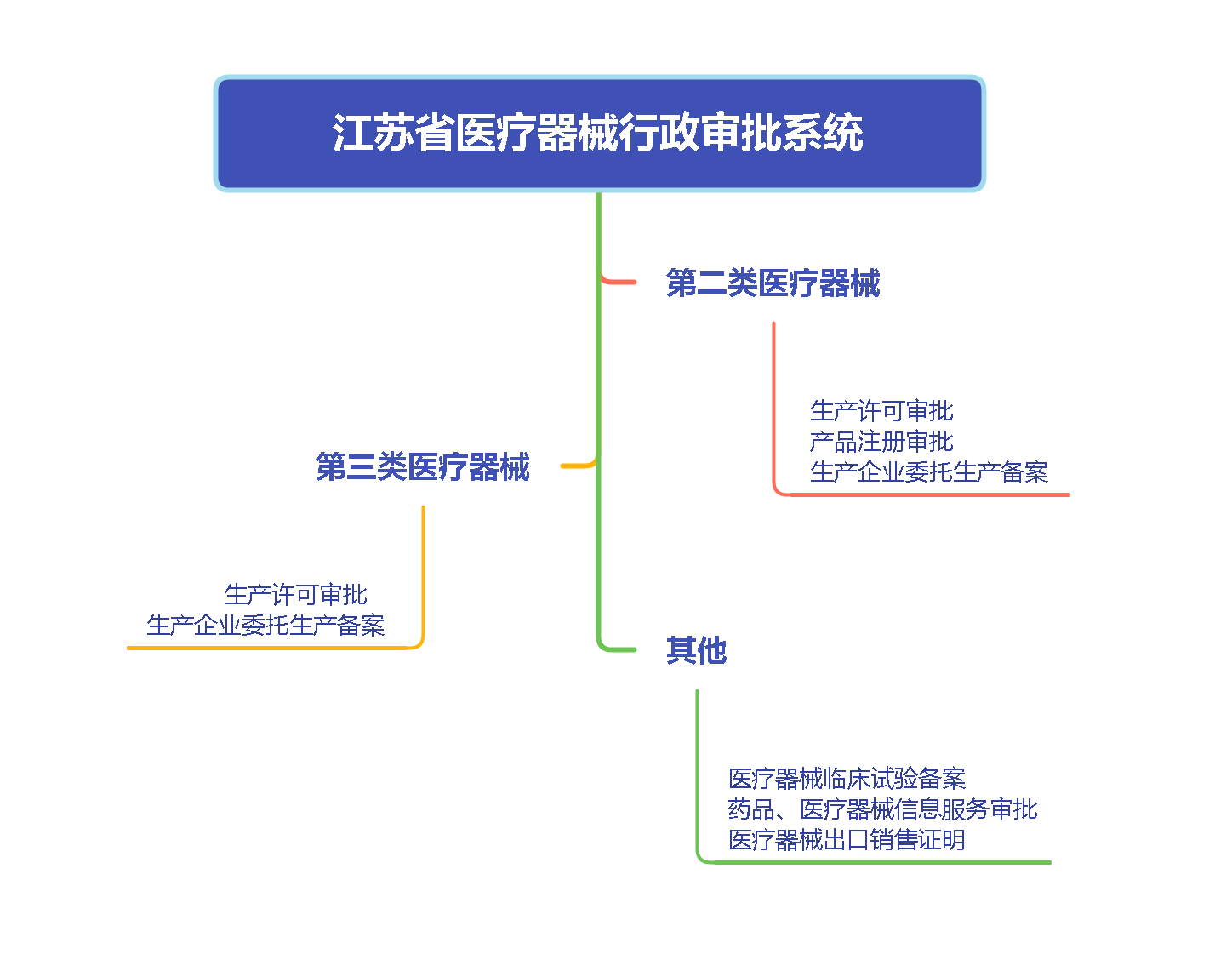
二、医疗器械注册电子申报的优势
与eRPS同期上线运行的还有新审评系统和审评项目智能化分配程序。这两系统+一程序的组合完美实现了简单审评项目与复杂审评项目分级、临床导向审评分段、项目管理人、项目小组审评、立卷审查等制度的有机融合,确保了分配准确性和时效性,提升了审评科学性,提高了审评审批效率,节约了时间成本。
三、医疗器械注册电子申报的有关要求
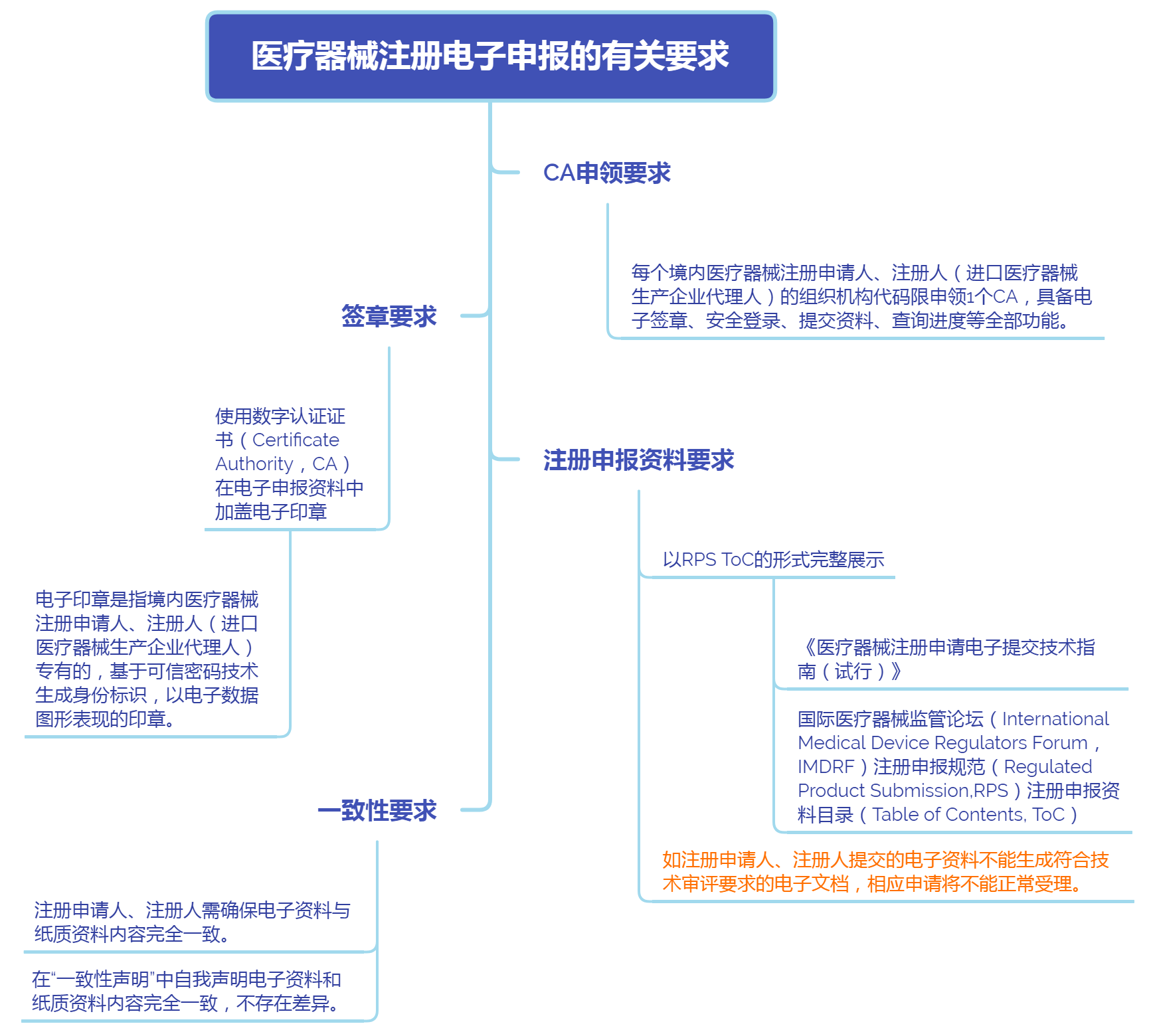
四、医疗器械注册电子申报相关文件及通知
2019.6.17
器审中心发布《关于医疗器械电子申报(eRPS系统)工作对外咨询服务的通知》
对医疗器械电子申报(eRPS系统)工作对外咨询服务进行通知,解决行政相对人操作层面的具体问题。
相关链接:
1.关于医疗器械电子申报(eRPS系统)工作对外咨询服务的通知
2019.6.06
器审中心发布《关于医疗器械注册电子申报信息化系统业务办理有关事宜的通告》(2019年 第4号)
对医疗器械电子申报信息化系统业务办理事宜进行通告,并对注册电子申报资料的提交过程进行说明。
相关链接:
1.关于医疗器械注册电子申报信息化系统业务办理有关事宜的通告(2019年第4号)
2019.6.06
器审中心发布《关于医疗器械注册电子申报信息化系统电子申报目录文件夹结构的通告》(2019年 第5号)
对医疗器械注册申请电子申报目录(RPS ToC)文件夹结构进行说明,方便行政相对人准备电子版注册申报资料。
相关链接:
1.关于发布医疗器械注册电子申报信息化系统电子申报目录(RPS ToC)文件夹结构的通告(2019年第5号)
2.医疗器械注册电子申报信息化系统电子申报目录(RPS ToC)文件夹结构
2019.5.31
国家药监局发布《关于实施医疗器械注册电子申报的公告》(2019年 第46号)
对医疗器械注册电子申报有关事项进行公告,并对适用范围及时间安排做出说明。
相关链接:
1.关于实施医疗器械注册电子申报的公告(2019年第46号)
2019.5.31
国家药监局发布《关于医疗器械注册申请电子提交技术指南的通告》(2019年 第29号)
对医疗器械注册申请电子提交技术指南进行通告,并对各类注册电子申报资料上传目录要求做出说明。
相关链接:
1.关于发布医疗器械注册申请电子提交技术指南的通告(2019年 第29号)
2019.5.07
器审中心发布《关于医疗器械注册电子申报信息系统数字认证(CA)证书申领有关事宜的通知》
对医疗器械注册电子申报信息系统数字认证证书申领和使用等事宜进行说明。
相关链接:
1.关于医疗器械注册电子申报信息系统数字认证(CA)证书申领有关事宜的通知
江苏省医疗器械行政审批系统通告
2020.4.26
相关链接:
五、医疗器械注册电子申报的常见问题
相关链接:
2.医疗器械注册电子申报信息系统数字认证(CA)证书申领的系列问答
六、医疗器械电子检测报告的相关事项
如今云时代已来临,为响应国家推行检测认证电子报告制度的号召,苏州大学卫生与环境技术研究所于2020年1月1日起在医疗器械领域推行电子检测报告。
质量办 :0512-65882617 quality@sudatest.com
医疗器械事业部: 0512-65880038 med@sudatest.com
【文章来源】国家药品监督管理局、国家药品监督管理局医疗器械技术审评中心、江苏省药品监督管理局
【全文整理】苏州大学卫生与环境技术研究所
【声明】如果您认为我们的内容或来源标注与原文不符,请告知我们,我们将与您积极协商解决。谢谢大家的关注!